Авторы статьи:
Е. Ильялова, врач-дерматовенеролог, косметолог, ведущий специалист компании Premium Aesthetics в области IPL и лазерных методик
И. Серегина, кандидат филологических наук, колумнист, специалист по связям с общественностью компании Premium Aesthetics Москва, Россия
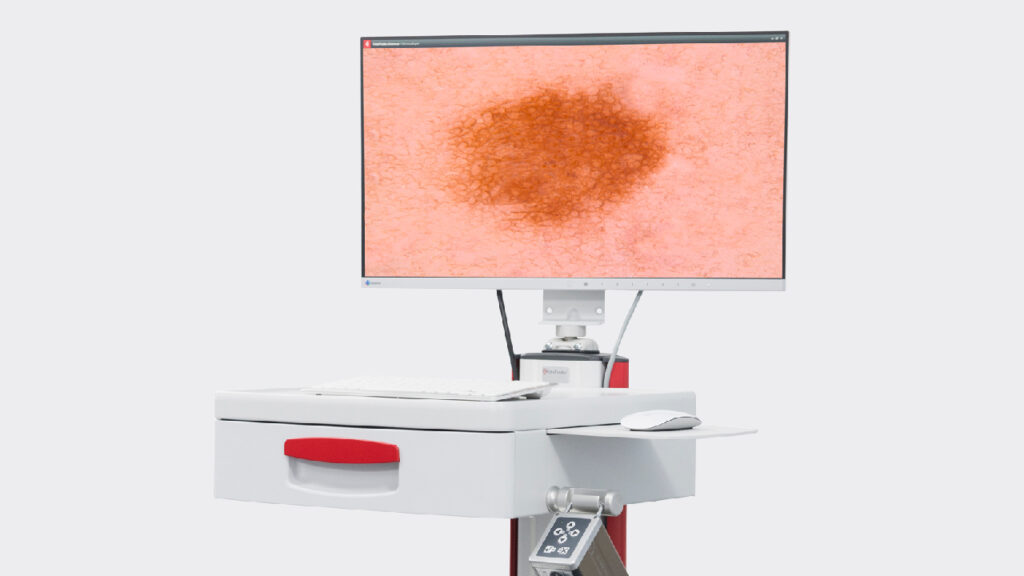
Дерматоскопия (греч. derma – кожа + skopeo – рассматривать, исследовать) традиционно определяется как неинвазивный метод исследования кожи с помощью оптического прибора дерматоскопа, широко применяемый при диагностике новообразований кожи в дерматологии и онкодерматологии. Основанный на увеличении изображения, этот эффективный метод позволяет оценить морфологическую структуру, выявить признаки злокачественности новообразования и незаменим, в частности, при диагностике меланомы на ранней стадии ее формирования.
Как вид визуального исследования дерматоскопия усложнялась в ходе своего развития. Современная высокоточная дерматоскопия предполагает использование цифровых дерматоскопов с функцией автоматического тотального картирования тела, в ходе которого за несколько минут можно составить «паспорт кожи» пациента.
Благодаря развитию телемедицины, обеспечивающей возможность удаленной консультации с экспертом, а также применению в медицине обучаемых нейросетей искусственного интеллекта (CNN глубинного обучения), сегодня наступает новая эра в диагностике злокачественных новообразований кожи.
Одним из первых о дерматоскопии как методе упоминал в своих исследованиях кровеносных сосудов ногтевого ложа Johan Ch. Kolhaus в XVII веке [1].
С конца XIX века для увеличения плотности контакта линзы с кожей в микроскопии стали использовать иммерсионную жидкость в качестве среды, которая выравнивает коэффициент преломления света [2]. Благодаря этому исследователи могли легко идентифицировать все существенные структурные компоненты новообразования уже при 10-кратном увеличении. И хотя до начала ХХ века способ осмотра кожных покровов пациента с помощью обыкновенной лупы все еще применяли, первые попытки добавить к увеличительному стеклу дополнительный встроенный источник света, а затем и создавать приборы, похожие на микроскоп, кардинально изменили существовавший взгляд на дерматоскопию.
Первые монокулярные и бинокулярные микроскопы для капилляроскопии, которые стали изготавливать начиная с 1916 года по чертежам O. Muller [3], быстро получили признание у исследователей. Значимый вклад в становление дерматоскопии как метода микроскопии кожи внес J. Saphier. В 1920 году он опубликовал результаты научно- исследовательской работы по диагностическому применению бинокулярного микродерматоскопа со слабым боковым источником освещения у больных с патологией кожи [4].
В 1950-х годах Dr. Goldman (США) продолжил популяризировать дерматоскопию, применяя приборы собственной разработки для исследования дерматозов, опухолей кожи и меланоцитарных невусов [5]. Об эффективности метода при дифференциальной диагностике доброкачественных и злокачественных опухолей в 1971 году писал R. MacKie [6]. С тех пор и до настоящего времени было проведено большое количество исследований для установления дерматоскопическо-гистологических корреляций и поиска универсальных диагностических алгоритмов.
Портативный бинокулярный стереомикроскоп с 10–40-кратным оптическим увеличением был разработан в 1990 году Kreusch и Rassner [7], а вскоре благодаря группе ученых во главе с O. Braun-Falco появился первый ручной образец дерматоскопа [8].
Появление новых, более сложных устройств для поверхностной микроскопии кожи диктовало необходимость выработки общего алгоритма для дифференциальной диагностики меланоцитарных и немеланоцитарных пигментных новообразований.
Первый дифференциально-диагностический алгоритм (pattern analysis), представленный в 1987 году группой ученых во главе с H. Pehamberger, был основан на изучении дерматоскопических признаков доброкачественных и злокачественных пигментированных опухолей кожи [9].
Немногим позднее в Гамбурге на Первой рабочей встрече по проблемам дерматоскопии были приняты рекомендации, включавшие список дерматоскопических признаков меланомы кожи, к которым была отнесена, в частности, неравномерная пигментная ретикулярная сеть, проявляющаяся участками регрессии пигментного новообразования, неравномерностью пигментации, наличием бело- голубой «вуали» и атипичных сосудов [10].
Начиная с 1994 года в клинической онкодерматологии применяется правило ABCDЕ (R. Friedman):
– А (asymmetry) – меланома кожи имеет вид асимметричного пигментного пятна (или папулы);
– B (border) – границы меланомы кожи неровные, нечеткие, могут иметь «географические очертания»;
– С (color) – для меланомы кожи характерна полихромия – наличие нескольких цветов в одном образовании;
– D (diameter) – диаметр меланомы кожи чаще всего превышает 0,5 см;
– E (evolution, elevation – эволюция, возвышение) – для меланомы кожи всегда характерна какая-либо эволюция с течением времени.
В своей работе, опубликованной в 1998 году, G. Argenziano представил «правило 7 признаков» [11]. В основу этого диагностического алгоритма было положено рандомизированное исследование 342 меланоцитарных новообразований кожи (117 меланом и 225 клинически атипичных невусов). Дерматоскопические признаки меланомы делят на большие (с весовым коэффициентом 2 балла) и малые (с весовым коэффициентом 1 балл). Если сумма баллов составляет 3 условные единицы и более, меланома выявляется с чувствительностью 95 и специфичностью 75%.
Дерматоскопия сегодня стала высокоточной благодаря цифровым дерматоскопам. Среди областей их применения можно выделить:
– дифференциальную диагностику новообразований кожи меланоцитарной и немеланоцитарной природы;
– раннюю диагностику меланомы;
– диагностику дерматозов, в т.ч. паразитарной и вирусной этиологии;
– диагностику состояния ногтей;
– диагностику волосистой части головы (трихоскопию);
– оценку эффективности терапии.
Современные дерматоскопы – уже не просто оптические устройства, но сложные программно- аппаратные комплексы, которые позволяют врачу изучать новообразования, делать цифровые фотографии и анализировать их с помощью специального программного обеспечения с использованием искусственного интеллекта.
Цифровая дерматоскопия существенно облегчает работу врача, незаменима для начинающего специалиста и помогает минимизировать случаи гипо- и гипердиагностики. Например, цифровой видеодерматоскоп последнего поколения оснащен автофокусом и оптическим зуммом до 140 крат, обеспечивает мгновенный захват изображений и подходит для любых видов дерматоскопических исследований и флуоресцентной диагностики (рис. 1).
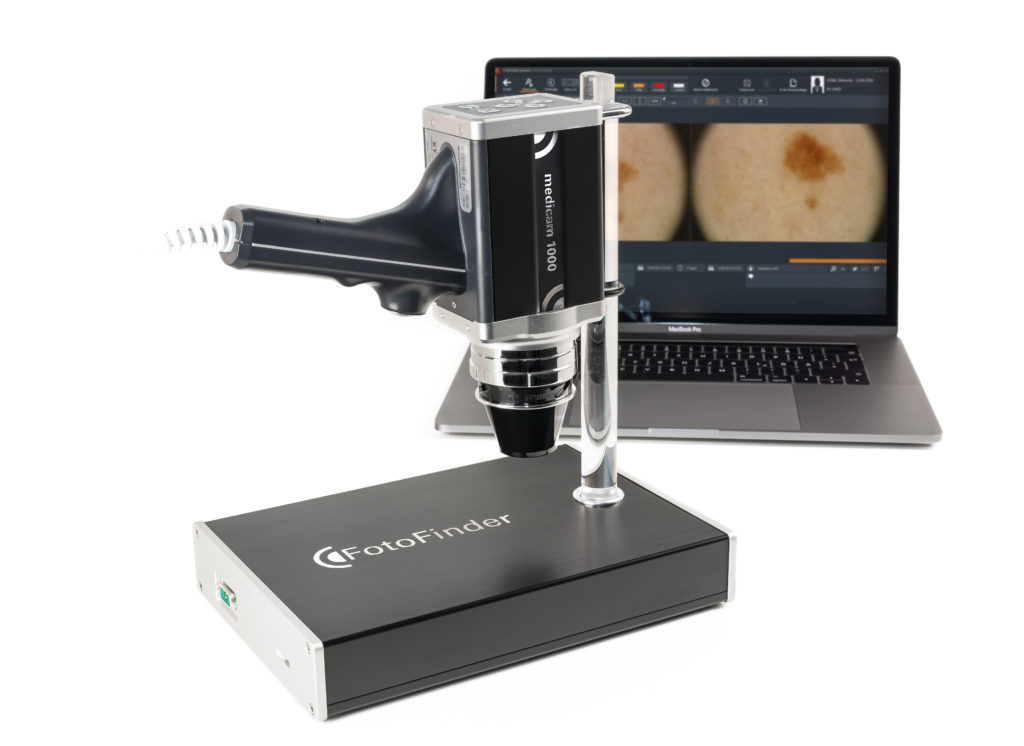
Рис. 1. Цифровой дерматоскоп последнего поколения
Среди преимуществ цифровой дерматоскопии следует отметить короткое время осмотра одного новообразования и объективизацию динамического наблюдения за растущими образованиями. Такое оборудование и программное обеспечение удобно для проведения скрининговых осмотров.
Однако даже с появлением высоких технологий в дерматоскопии количество диагностических ошибок остается высоким. По имеющимся данным, частота ошибок клиницистов в распознавании меланомы варьируется от 18 до 81%, при этом даже гистологическое исследование дает до 20–30% ошибочных результатов. Это отражается на тактике лечения, что приводит как к гипердиагностике, так и к появлению запущенных случаев с неблагоприятным исходом. По-прежнему большое значение в диагностике меланомы имеют квалификация и опыт врача первичного звена [12].
Учитывая существенный рост заболеваемости злокачественными новообразованиями кожи и меланомой в России в последние годы, проблема ранней и высокоточной диагностики чрезвычайно актуальна. По официальным данным Минздрава РФ, в 2017 году было диагностировано 617 200 новых случаев злокачественных новообразований, среди них 89 000 случаев онкологических заболеваний кожи (14,4% от всех видов рака), в т.ч. 11 200 случаев меланомы (12,5%), помимо меланомы – 78 000 случаев (87,5%). При этом высок уровень запущенности меланом, диагностированных впервые: 19,1% меланом, диагностированных в 2018 of the American Academy of Dermatology под названием Second primary melanomas in a cohort of 977 melanoma patients within the first 5 years of monitoring («Риск выявления вторичной меланомы у 977 пациентов экспериментальной группы с установленным диагнозом «меланома» в ходе 5-летнего мониторинга), подтверждена эффективность цифровой дерматоскопии и тотального картирования тела для диагностики и раннего обнаружения меланомы: из всех новых случаев заболевания меланомой 17,3% были диагностированы в ходе клинического и дерматологического осмотров, 48,1% – с помощью тотального фотокартирования тела и 34,6% – благодаря цифровой дерматоскопии.
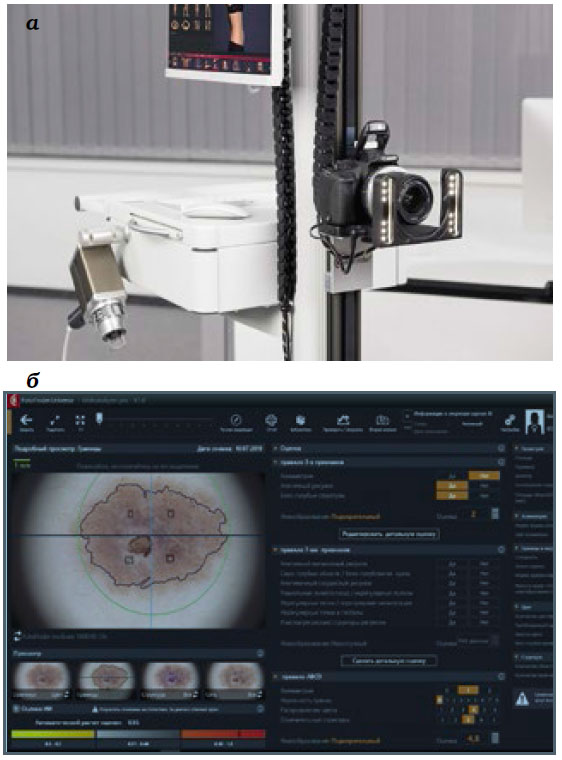
Рис. 2. Современный диагностический
программно-аппаратный комплекс для
автоматического картирования тела (а);
изображение новообразования, получаемое с его
помощью (б)
Фотокартирование представляет собой процесс создания серий фотоснимков поверхности тела пациента в разные периоды времени с последующим их сравнением и анализом. Автоматическое тотальное картирование тела (Automated Total Body Mapping, ATBM), – наиболее удобный, точный и быстрый метод диагностики. Снимки всех новообразований на теле пациента можно сделать за несколько минут, составив «карту новообразований кожи», и в режиме реального времени выявить степень их злокачественности. Снимки можно сохранить и распечатать по желанию пациента. Эта процедура незаменима для диагностики у пациентов с множественными невусами, поскольку позволяет наблюдать эволюцию каждого новообразования.
Еще одно нововведение – создание первого в мире карманного устройства для цифровой дерматоскопии – handyscope, работающего совместно с iPhone и существенно расширяющего возможности диагностики в дерматологии, онкологии и трихологии.
Среди последних достижений в области диагностики новообразований кожи необходимо упомянуть использование возможностей искусственного интеллекта (CNN глубинного обучения). Структура искусственной нейронной сети напоминает организацию нейронов в головном мозге. Искусственная нейросеть состоит из «виртуальных нейронов», каждый из которых представляет собой логический блок, получающий входную информацию, принимающий на ее основе решение и передающий информацию другим нейронам, получая по обратной связи их «вердикт» – верно ли принятое им решение или нет. Если решение верное, то данный «виртуальный нейрон» получает больший «вес» среди других нейронов сети и его последующие решения будут иметь большее значение. Если же решение оказалось неверным, «вес» «виртуального нейрона» в сети уменьшается. Нейроны искусственной сети организованы в слои (рис. 3). В каждом слое, т.е. на каждом уровне принятия решения в ходе «обучения», постепенно остаются нейроны, которые чаще находили верные решения, и исключаются те, чьи решения чаще оказывались неверными.
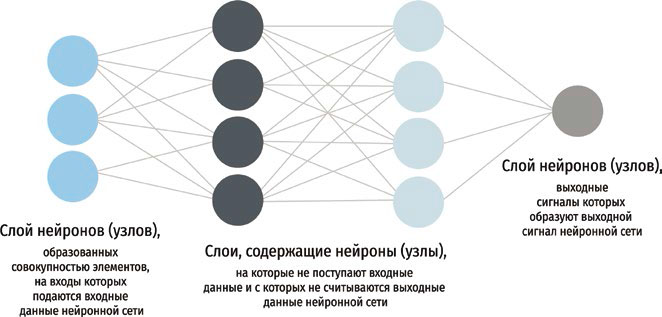
Рис. 3. Схема работы искусственной нейронной сети CNN
Искусственный интеллект на основе нейросетей активно используется в современной медицине для распознавания изображений. В дерматоонкологии с помощью сверхточных нейронных сетей глубинного обучения распознают изображения, полученные с помощью цифрового дерматоскопа или фотоаппарата [13, 14]. Так, в статье Man against machine: diagnostic performance of a deep learning convolutional neural network for dermoscopic melanoma recognition in comparison to 58 dermatologists («Человек против машины: сравнение результатов дерматоскопического распознавания меланомы, выполненного нейронной сетью глубинного обучения и 58 дерматологами») было показано, что эффективность распознавания меланомы сетью CNN превосходит возможности большинства дерматологов [15].
Наконец, крайне перспективным представляется использование опции видеозаписи макро- и микроизображений, доступной в обновленной версии программного обеспечения для цифрового дерматоскопа. Качество получаемого таким образом изображения не зависит от обстоятельств съемки (например, от того, насколько равномерно распределилась под стеклом иммерсионная жидкость, хорошо ли прижаты структуры на поверхности кожи и др.). Такие короткие видеоролики, созданные в формате Full HD, можно не только просматривать, но и сравнивать один с другим при наблюдении за новообразованием в динамике.
Таким образом, можно отметить, что дерматоскопия как метод диагностики новообразований кожи с момента ее внедрения в клиническую практику претерпела значительные изменения. Сегодня область применения дерматоскопа обширна, а эффективность диагностики крайне высока. Совмещенный с искусственным интеллектом современный цифровой дерматоскоп – незаменимый инструмент в руках специалиста с любым опытом, позволяющий диагностировать злокачественные новообразования кожи, в т.ч. меланому, на самой ранней стадии.
Литература
1. Gilje O, O’Leary PA, Baldes EY. Capillary microscopic examination in skin disease. Arch Dermatol, 1958;68:136–145.
2. Diepgen P. Geschichte der Medizin. – Berlin: de Gruyter. 1965. P. 138–153.
3. Muller O. Die Kapillaren der menschlichen Korperoberflache in gesunden und kranken Tagen. – Stuttgart: Enke, 1922.
4. Saphier J. Die Dermatoskopie. I. Mitteilung. Arch Dermatol Syphiol, 1920;128:1–19.
5. Goldman L. Some investigative studies of pigmented nevi with cutaneous microscopy. J Invest Dermatol, 1951;16:407–427.
6. MacKie R. An aid to the preoperative assessment of pigmented lesions of the skin. Br J Dermatol, 1971;85:232–238.
7. Kreusch J, Rassner G. Strukturanalyse melanozytischer Pigmentmale druch Auflichtmikroskopie. Hautarzt, 1990;41:27–33.
8. Braun-Falco O, Stolz W, Bilek P, et al. Das Dermatoskop. Eine Vereinfachung der Auflichtmikroskopie von pigmentierten Hautveranderungen. Hautarzt, 1990;41:131–136.
9. Pehamberger H, Steiner A, Wolff K. In vivo epiluminescence microscopy of pigmented skin lesions. I. Pattern analysis of pigmented skin lesions. J Am Acad Dermatol, 1987;17:571–583.
10. Bahmer FA, Fritsch P, Kreusch J, et al. Terminology in surface microscopy. J Am Acad Dermatol, 1990;23:1159– 1162.
11. Argenziano G, Fabbrocini G, Carli P, et al. Epiluminescence microscopy for the diagnosis of doubtful melanocytic skin lesions. Comparison of the ABCD rule of dermatoscopy and a new seven-point checklist based on pattern analysis. Arch Dermatol, 1998;134:1563–1570.
12. Дерматоонкология (злокачественные новообразования кожи, первичные лимфомы кожи): Атлас. Под общ. ред. проф. Кунгурова НВ. – Екатеринбург: Макс-Инфо, 2016. С. 68–69.
13. Dormehl L. What is an artificial neural network? Here’s everything you need to know. Digital Trends 2018. – www.digitaltrends.com/cool-tech/what-is-an-artificialneural- network.
14. Краюшкин ПВ. Возможности искусственного интеллекта в диагностике онкологических заболеваний кожи. Косметика и медицина, 2018;(3):90–99.
15. Alt C, Arenbergerova M, Bakos R, et al. Man against machine: diagnostic performance of a deep learning convolutional neural network for dermoscopic melanoma recognition in comparison to 58 dermatologists. J Am Acad Dermatol, 2020;82(Issue 2):398–406. – https:// www.sciencedirect.com.