Gabriel Salerni, MD,a Cristina Carrera, MD,a,b Louise Lovatto, MD,a Joan Anton Puig-Butille, PhD,b
Celia Badenas, PhD,b,c Estel Plana,d Susana Puig, MD, PhD,a,b and Josep Malvehy, MD, PhDa,b Barcelona, Spain
Раннее выявление меланомы — важнейший фактор в улучшении прогноза ее развития. Цифровые методы обследования населения из группы высокого риска являются эффективным способом выявления меланомы, позволяющим избежать осложнений.
Мы намерены сообщить о значимости двухступенчатого метода исследования (тотального фотографирования тела и цифровой дерматоскопии).
В настоящем исследовании приведен анализ результатов наблюдений за 618 пациентами с высоким риском меланомы, проводившегося в рамках программы цифрового исследования DFU в период с 1999 по 2008 гг.
В ходе исследования проводилось наблюдение в общей сложности 11 396 новообразований (среднее значение 18,44 на пациента) в среднем в течение 96 месяцев (в среднем 10 приемов на пациента). В общей сложности 1 152 новообразований, в среднем 1,86 на пациента, были иссечены. Почти 70 % (798) новообразований были ранее зафиксированы по крайней мере дважды, из них 356 (30 %) были выявлены и удалены на том же приеме. В ходе исследования 98 меланом (8,5 % иссеченных новообразований) были диагностированы у 78 пациентов (12,6 %). В общей сложности 53 выявленные меланомы были in situ, и 45 с уровнем инвазии согласно классификации по Бреслоу менее 1 мм (в среднем 0,5 мм), и ни одна из них не была изъязвленной.
Ограничения
Поскольку контрольных групп в исследовании не было, мы не можем определить, является ли сочетание двух методов — тотального картирования и цифровой оценки ― более эффективным, чем каждый из методов по отдельности.
Метод цифровой оценки DFU с тотальным картированием и дерматоскопией в выбранной группе с высоким риском меланомы показывал ранее выявление меланомы с низким уровнем иссечений. Для выявления медленно растущих меланом требуется долгосрочная оценка. Основываясь на нашем 10-летнем опыте, меланому можно диагностировать в любое время, при этом в группе высокого риска требуется наблюдение в динамике (J Am Acad Dermatol 2012;67:e17-27).
Преимущества тотального картирования тела и цифровой дерматоскопии («двухступенчатый метод цифровой оценки») в ранней диагностике меланомы у пациентов с высоким риском заболевания Salerni et al 2 J AM ACAD DERMATOL JULY 2012
КЛЮЧЕВЫЕ СЛОВА: синдром атипичного (диспластического) невуса, дерматоскопия, наблюдение, методы визуализации, злокачественная меланома, результат.
Источники финансирования
Исследование в Барселоне частично финансировалось грантами 03/0019, 05/0302 и 06/0265, предоставленными фондом Fondo de Investigaciones Sanitarias, Испания; а также CIBER de Enfermedades Raras of the Instituto de Salud Carlos III, Испания; Ag_encia de Gesti_o d’Ajuts Universitaris i de Recerca (AGAUR) 2009 SGR (Suport a grups de recerca) 1337 Правительства Каталонии, Испания; European Commission under the Sixth Framework Programme, по контракту No. LSHC-CT-2006-018702 (GenoMEL); и National Cancer Institute of the US National Institutes of Health (CA83115). Спонсоры не влияли на структуру и проведение исследований, сбор, анализ и интерпретацию данных, подготовку, рассмотрение или одобрение отчета.
Конфликт интересов
Не сообщалось.
Злокачественная меланома может быть неотличимой от меланоцитарного невуса клиническими и дерматоскопическими методами, что делает раннюю диагностику необходимой, особенно в отношении новообразований¹ на ранних стадиях развития. Дерматоскопическое исследование меланоцитарных невусов путем сравнения их состояния в динамике, известное как цифровая оценка, является полезным в диагностике ранней меланомы, когда критерий злокачественности меланомы еще не применим². Использование исходных изображений тотального картирования тела (TBM) может повысить степень выявления вновь появившихся новообразований и визуальных изменений, имевшихся ранее невусов, определяя участки для последующего наблюдения³. Тем не менее предполагается, что стратегия визуализации, сфокусированная только на атипичных невусах, может привести к неверной диагностике в случаях, если меланома проявится во вновь появившихся невусах или относится к новообразованиям, не подлежащим определению цифровым методом⁴.
Нашей группой было предложено совместное применение тотального картирования тела и цифровой дерматоскопии, так называемого «двухступенчатого метода»⁵, как метода наблюдения пациентов с повышенным риском заболевания, потенциально более точного, чем два метода по отдельности. Это исследование направлено на демонстрацию нашего 10-летнего опыта работы в отделении меланомы (Melanoma Unit of Hospital Clinic of Barcelona, Испания) с использованием последних методов проспективного наблюдения пациентов с высоким риском меланомы, включенных в нашу специальную программу наблюдений. Наше исследование не только подтверждает открытия, сделанные другими исследовательскими группами, но также предоставляет новые данные, основанные на долгосрочном наблюдении, более чем в два раза превышающем сроки других исследований⁶,⁷ и включающем более 600 пациентов с более чем 11 000 новообразованиями.

В программу наблюдений с применением тотального картирования тела TBM и цифровой дерматоскопии, проводимой в отделении меланомы (Melanoma Unit of Hospital Clinic of Barcelona, Испания), в период с января 1999 по декабрь 2008 года были включены в общей сложности 629 пациентов. Критерием включения в исследование были: от умеренных до выраженных проявлений синдрома атипичного (диспластического) невуса (более 100 невусов и/или >10 клинически атипических, согласно правилам ABCD, и/или гистологически определенных диспластических невусов), наличие злокачественной меланомы в личном или семейном анамнезе, носители мутации генов или иные факторы риска, включая наличие врожденных невусов среднего и большого размера, иммуносупрессию, генодерматоз (например, ксеродерма пигментная, синдром Горлина-Гольца), связанные или не связанные с синдромом атипичного (диспластического) невуса.
Пациенты, включенные в программу, должны были проходить как минимум по 2 контрольных осмотра в течение 12 месяцев. В общей сложности 11 пациентов были исключены на начальном этапе, поскольку не выполняли это условие. Исследование проводилось в соответствии с Хельсинкской декларацией и имело институциональное одобрение.
Пациент подписывал информированное согласие на проведение всех инвазивных процедур.
Первичные и контрольные данные
На первичном приеме собиралась полная клиническая картина жизни участника, включая семейный анамнез, ранее удаленные меланоцитарные новообразования и другие факторы риска.
Первичное цифровое обследование состояло из двух ступеней. Первая — тотальное картирование тела для обследования и визуализации, и вторая — цифровая дерматоскопия новообразований в реальном времени. Производилось сохранение всех снимков с проявлением признаков атипичности. Тотальное картирование в стандартизированных условиях проводилось по двухступенчатому методу⁵, разработанному нашей группой.
Контрольное обследование включало: первую ступень (тотальное картирование тела) для сравнения снимков, произведенных на предыдущих осмотрах, для определения изменения формы, цвета, структуры в любом пигментном новообразовании и для выявления вновь появившихся новообразований, и вторую ступень (цифровая дерматоскопия) для дерматоскопического сравнения и фиксации новообразований с атипичными признаками, клинического и дерматоскопического исследования новообразований, не зарегистрированных ранее. Контрольные осмотры, включавшие только вторую ступень — цифровую дерматоскопию, без тотального картирования тела, производились при наблюдении за выбранными пациентами с низким или умеренным риском или для мониторинга развития специфических новообразований.
Каждое обследование проводилось экспертом в области дерматологии в течение 30–45 минут. Съемка производилась при помощи цифровой системы (MoleMax, Derma Instruments, Вена, Австрия). Контрольные осмотры назначались через 3, 6, 12 месяцев, в зависимости от рекомендаций врача, проводившего осмотр. Краткосрочный контроль (через 3 месяца) назначался при наличии подозрительных меланоцитарных новообразований, которые не отвечали дерматоскопическим критериям выявления меланомы, тогда как среднесрочный и долгосрочный (через 6 и 12 месяцев) контрольный осмотр назначался пациентам с высоким или умеренным риском соответственно, согласно критериям включения в исследование.
Меланоцитарные новообразования с атипичными клиническими или дерматоскопическими признаками фиксировались в цифровой базе данных. Новообразования с явными признаками злокачественной меланомы (согласно анализу характеристик⁸, правилам дерматоскопии ABCD⁹, или 7-пунктовому чек-листу¹⁰) не фиксировали, как и новообразования с очевидными дерматоскопическими признаками доброкачественности. Новообразования, признанные подлежащими удалению сразу после первых обследований, не анализировались, поскольку не были частью исследования: 16 злокачественных меланом были выявлены у 14 пациентов при первичном осмотре.
Любое новообразование, демонстрировавшее следующие изменения, выявленные в ходе цифровой дерматоскопии, иссекалось и отправлялось на гистопатологическое исследование: (1) асимметричное увеличение размера; (2) изменение дерматологической структуры (форма, увеличение или сокращение пигментной сетки, изменения в распределении пигмента, частиц; видоизменение депигментированных участков или структур; появление прожилок, рубцеподобных участков, появление диффузной бело-голубой вуали, атипичных сосудов) (3) увеличение количества цветов; (4) признаки регрессии на 50 % поверхности новообразования; (5) точечные пигментные изменения. Все новые или ранее не зарегистрированные новообразования, выявленные на контрольных осмотрах и имеющие признаки атипии, но не соответствующие критериям злокачественной меланомы, фиксировались и использовались при контрольных обследованиях; новообразования, соответствовавшие критериям злокачественности, исключались. В общей сложности 22 доброкачественных новообразования были удалены исходя из практического и эстетического критериев, основываясь на мнении пациента или врача. Поскольку они не считались относящимися к атипичным меланоцитарным новообразованиям, не признавались злокачественной меланомой и не являлись частью контрольного обследования, они исключались из исследования. Все эти новообразования в ходе гистопатологического исследования были признаны доброкачественными.
Все удаленные новообразования были разделены на срезы и отправлены на стандартное гистопатологическое исследование. Проводилась стандартная окраска гематоксилин-эозином и иммуно-гистохимическое исследование (Melan A, HMB-45 [human melanoma black 45, Ki67]), при необходимости также двумя патологами. Гистологические критерии атипии сообщались в соответствии с Консенсусом Собрания национальных институтов здоровья США 1992 года (National Institutes of Health Consensus Conference).
После подписания пациентами информированного согласия и разъяснения им содержания исследования проводилось генетическое тестирование тех участников с личным и/или семейным анамнезом множественных меланом. Экзон 1 альфа, 1 бета, 2,3; мутации гена IVS2-105 и -34G<T гена CDKN2A, и CDK4 экзон 2 изучались посредством ПЦР с анализом конформационного полиморфизма одноцепочечных фрагментов ДНК и последовательности. Ген MC1R исследовался методом прямой последовательности, как сообщалось ранее¹¹.
Соответствие пациентов оценивалось согласно продолжительности программы наблюдения. Были определены пациенты, исключенные из программы, но продолжавшие клиническое и дерматоскопическое обследование, покинувшие программу или умершие.
Бивариантный анализ проводился для оценки различий у пациентов, которым был поставлен диагноз меланомы во время контрольного наблюдения и кому не был; критерий согласия X2 использовался для сравнения качественных различий с применением критерия Фишера исходя из потребности выборки 2×2 и t-теста Стьюдента для сравнения средних значений качественных показателей. Разница считалась статистически значимой, если P был ниже 0.5. Анализ методом многофакторной логистической регрессии использовался для получения отношения шансов с использованием прямого подхода, включая в модель одну переменную с P ниже 0.2 за другой в бивариантном анализе.
В программе наблюдений принимали участие 618 пациентов, средний возраст которых во время вступления в программу составлял 37 лет (среднее стандартное отклонение ± 13,3); 45,5 % были представителями мужского пола. Согласно критериям включения в исследование, большинство пациентов (n=556) страдали синдромом атипичного (диспластического) невуса, и только 7,1 (n=44) имели менее 50 невусов, ассоциированных с высоким риском. В нашей клинике наблюдались 277 пациентов, имевших в личном анамнезе злокачественную меланому, в том числе 73 пациента со множественными злокачественными меланомами до начала исследования; 8 пациентов, страдавших врожденным гигантским меланоцитарным невусом, и 3 пациента с пигментной ксеродермой. Почти треть пациентов (n=178) также имели семейный анамнез злокачественной меланомы. Описательные данные относительно количества невусов, фототипа кожи, цвета глаз, волос, лентигиноза и наличия генетических мутаций приведены в Таблице I.
Пациентов наблюдали в среднем по 96 месяцев (от 13 до 120 месяцев). В течение 10 лет наблюдений были проведены 6149 осмотров (4155 с тотальным картированием тела и 1994 методом цифровой дерматоскопии). Каждый пациент за время наблюдения обследовался в среднем 10 раз (от 2 до 22), в том числе 7 раз (от 2 до 17) с применением тотального картирования тела и цифровой дерматоскопии, и 3 промежуточных осмотра (0-11) только методом цифровой дерматоскопии. Во время исследования 78 070 записей картирования (в среднем 126,3 на пациента, от 9 до 410) и 88 283 цифровых снимков (в среднем 142,9 на пациента, 6–726) были сохранены в базе данных.
Таблица 1. Описательные данные об участниках
| Возраст на дату вступления в исследование | 37 (среднее стандартное отклонение ±13,3) |
| Пол | |
| Мужской | 281 (45,5 %) |
| Женский | 337 (54,5 %) |
| Личный анамнез на дату вступления в исследование | |
| Меланома | 28 (4,53 %) |
| Меланома и Синдром атипичного (диспластического невуса) | 245 (39,64 %) |
| Синдром атипичного (диспластического невуса) | 311 (50,32 %) |
| Пигментная ксеродерма (все имели злокачественную меланому ранее) | 3 (0,5 %) |
| Гигантский врожденный невус (1 имел злокачественную меланому ранее) | 8 (1,29 %) |
| Другие (например, с семейным анамнезом злокачественной меланомы, с синдромом Горлина-Гольца) |
23 (3,72 %) |
| Количество невусов | |
| <50 | 44 (7,11 %) |
| 50–100 | 218 (35,30 %) |
| 100–200 | 241 (38,99 %) |
| >200 | 115 (18,60 %) |
| Фототип | |
| I | 19 (3,1 %) |
| II | 249 (40,3 %) |
| III | 327 (52,9 %) |
| IV | 23 (3,7 %) |
| V | 0 |
| VI | 0 |
| Цвет глаз | |
| Голубые | 80 (12,9 %) |
| Зеленые | 76 (12,3 %) |
| Карие | 445 (72,0 %) |
| Черные | 17 (2,8 %) |
| Цвет волос | |
| Рыжие | 26 (4,2 %) |
| Каштановые | 84 (13,6 %) |
| Светлые | 463 (74,9 %) |
| Черные | 45 (7,3 %) |
| Лентигиноз | |
| Средний | 209 (33,8 %) |
| Умеренный | 97 (15,7 %) |
| Выраженный | 72 (11,7 %) |
| Отсутствует | 240 (38,8 %) |
| Мутации гена CDKN2A | 39 (11,5 % обследованных) |
| Полиморфизм гена MC1R | 163 (75,1 % обследованных) |
| V60L | 42 |
| М92 | 17 |
| К151С | 28 |
В общей сложности наблюдались 11 396 новообразований, в среднем 18,44 на пациента (1–60). Среди них 1152 новообразований, в среднем 1,86 на пациента, были иссечены и отправлены на гистопатологическое исследование в ходе программы наблюдения. У 211 пациентов иссечение не требовалось, и у 149 иссекалось только одно новообразование за 10 лет исследования. Таким образом, почти у 60 % участников не требовалось удаление новообразований или требовалось иссечение только одного. В то же время за время программы исследования 7 пациентам потребовалось 10 и более иссечений. Но это были те участники, в чьем личном или семейном анамнезе присутствовали множественные злокачественные меланомы в начальной стадии, а также носители мутаций гена CDKNA2A или пациенты, страдающие пигментной ксеродермой.
Среди удаленных во время контрольных осмотров новообразований 779 (67,7 %) были зафиксированы ранее и находились под наблюдением, и 373 (32,4 %) были вновь выявлены на контрольных осмотрах или присутствовали ранее, но не требовали цифрового контроля. Гистопатологический диагноз меланоцитарных и немеланоцитарных новообразований (изначально предполагавшихся меланоцитарными и потому зафиксированными для цифрового наблюдения) иссекались в обеих группах, как показано на Рисунке 1.
Во время цифрового исследования у 78 пациентов были выявлены 98 меланом (8,5 % иссеченных, отношение доброкачественные/злокачественные составляло 10,7:1); 60 злокачественных мела- ном находились под наблюдением (7,7 % зарегистрированных новообразований, отношение доброкачественные/злокачественные — 11,9:1) (Рисунок 2) и 38 не были зафиксированы ранее (10,2 % новых незафиксированных ранее новообразований с соотношением доброкачественные/злокачественные 8,8:1) (Рисунок 3).
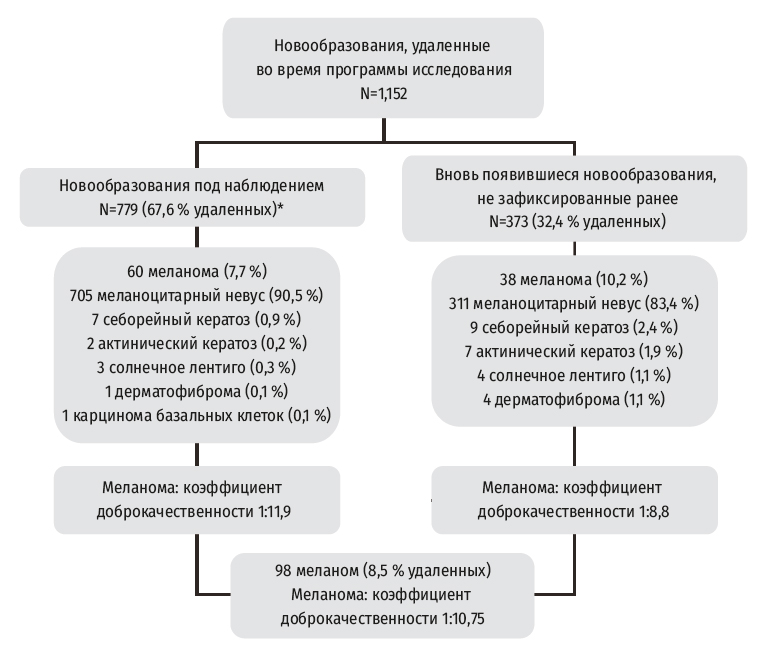
Рисунок 1. Новообразования, удаленные во время программы наблюдения.
*Относится к 6,8 % всех новообразований, находившихся под наблюдением
Выявление злокачественной меланомы путем анализа изменений, выявленных по данным цифровой дерматоскопии, потребовало в среднем 4 (2–15) контрольных осмотра со средней продолжительностью наблюдений 23,9 месяцев (1–77 месяцев); из них 16 злокачественных новообразований развивались на фоне имевшихся невусов, а 44 не имели связи с ранее существовавшими невусами согласно гистопатологическому исследованию. Гистопатологически 53 злокачественные меланомы были in situ (53,3 %); уровень инвазии по Бреслоу у других имевшихся новообразований составлял 0,5 мм (в среднем 0,62 мм), не было выявлено ни одной злокачественной меланомы толще 1 мм или с изъязвлением, то есть все злокачественные меланомы были стадированы по системе IA (American Joint Committee on Cancer 2009). В общей сложности 1015 меланоцитарных невусов были удалены в ходе программы исследования, почти половина из них характеризовалась определенной степенью гистологической атипичности (18,7 % — средние, 23,8 % — умеренные, 6 % — выраженные).
Согласно гистологическим исследованиям, 45,4 % демонстрировали регрессию, воспалительные изменения, невус Саттона или фиброз, что могло бы объяснить дерматоскопические изменения во время наблюдения.
В ходе контрольных осмотров 78 пациентам (12,6 %) диагноз злокачественной меланомы был поставлен при цифровом исследовании. Чаще всего это были мужчины (P=<02), которые были старше в начале исследования (P<.001), имели большее количество новообразований (P<.001) и большее количество новообразований, удаленных во время цифрового наблюдения, чем у тех, кому не ставился диагноз злокачественной меланомы; не было существенных различий в интервалах между осмотрами в двух группах.
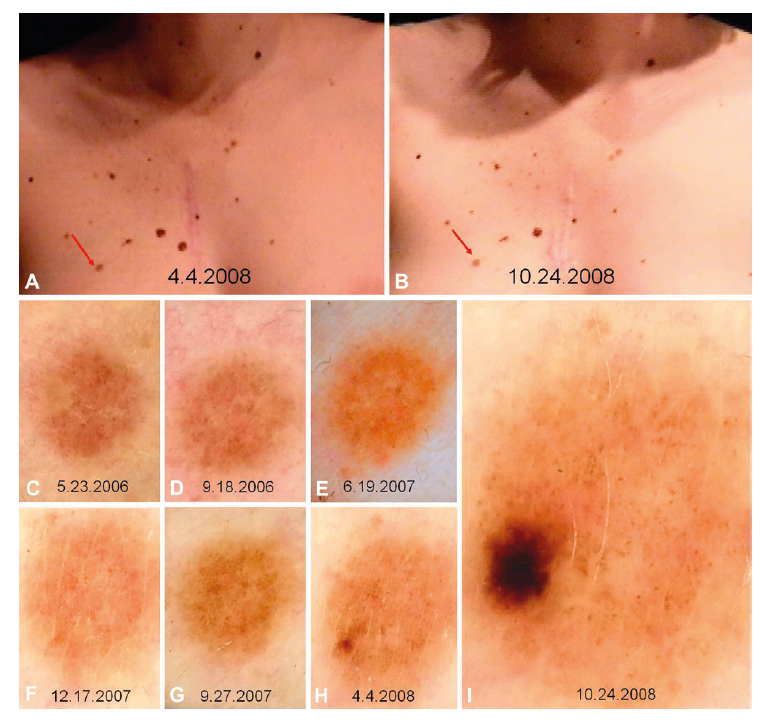
Рисунок 2. Меланома in situ, развившаяся над меланоцитарным невусом у 23 летней пациентки с личным и семейным анамнезом злокачественной меланомы; диагноз поставлен на основании изменений, выявленных во время цифровой дерматоскопии. Снимки тотального картирования тела не показывают клинических изменений (A и B), дерматоскопические данные в хронологическом порядке до момента удаления через 29 месяцев и 7 контрольных осмотров (С-I)
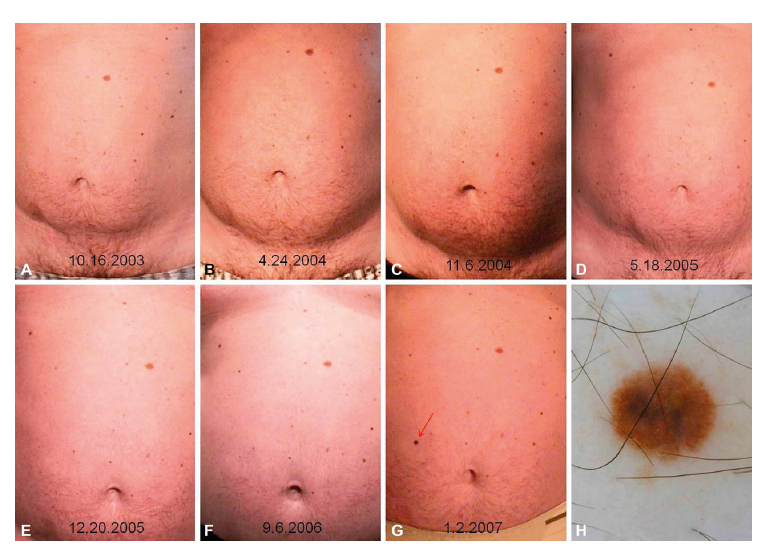
Рисунок 3. Поверхностная злокачественная меланома. Инвазия по Бреслоу 0,5 мм, уровень по Кларку III, выявлена как вновь появившееся новообразование при сравнении снимков зоны живота, произведенных при тотальном картировании тела у мужчины в возрасте 48 лет, носителя мутации гена CDKN2A, с личным и семейным анамнезом меланомы и синдромом атипичного (диспластического) невуса. Картирование тела показало появление новообразования (A-G), клинически симметричного с ровными границами. Дерматоскопический снимок (H) показывает атипичную пигментную сеть, инвертированную пигментную сеть, голубоватый оттенок.
Злокачественная меланома и множественные злокачественные меланомы в анамнезе у пациентов, которым во время исследования был поставлен диагноз, встречались чаще (P<.001 и =.003 соответственно), но не было установлено существенной зависимости от наличия злокачественной меланомы до исследований. Не было обнаружено статистически значимых различий в зависимости от количества невусов в 4 категориях (<50, 50–100, 100–200 и >200), но пациентам более чем с 100 невусами чаще ставили диагноз злокачественной меланомы, чем тем, у кого невусов было менее 100 (P=.007). Как ожидалось, у пациентов с синдромом атипичного (диспластического) невуса во время исследований выявляли больше злокачественных меланом, чем у тех, кто синдромом не страдал, но эта разница была незначительной (P=.636). Не было существенной зависимости от фототипа, наличия и степени лентигиноза, мутаций гена CDKN2A в двух группах (Таблица 2).
В анализе методом многофакторной логистической регрессии (Таблица 3) более старший возраст при вступлении в исследование и большее количество новообразований, иссеченных в ходе исследования, были переменными, чаще ассоциированными с диагностированием меланомы во время цифрового исследования (P=.003 и <.001 соответственно); мужской пол, наличие меланомы в прошлом или присутствие мутаций гена CDKN2A также ассоциировались с меланомой, диагностированной во время контрольных осмотров, но различия не были статистически значимыми. Фототип IV и отсутствие мутаций гена CDKN2A ассоциировались с низким риском меланомы (P=.033 и <.001 соответственно); фототипы II и III ассоциировались с более низким риском меланомы, чем тип I, но статистически значимых различий не наблюдалось (P=.123 и =.423 соответственно).
Что касается критериев соответствия цифровому исследованию, 519 пациентов (84,1 %) пациентов продолжают наблюдение в программе, 47 пациентов (7,6 %) были исключены из программы и продолжают клинические и дерматоскопические обследования в нашем отделении, 38 пациентов (6,1 %) покинули программу или были переведены в группу дерматологического наблюдения в другом центре, и 14 пациентов (2,2 %) умерли, в том числе 12 в результате развития злокачественной меланомы, один — вследствие инфаркта и один в результате мышечной дистрофии Душена.
Таблица 2. Различия между пациентами с поставленным во время контрольного наблюдения диагнозом злокачественной меланомы и без него. Злокачественная меланома во время контрольного наблюдения НЕТ (N=540) ДА (N=78)
| N (кол-во) | % | N (кол-во) | % | P Значение | OR | 95 % CI | |
| Пол | |||||||
| Мужской | 304 | 56,3 | 33 | 42.3 | .020 | 1.00 | Референс |
| Женский | 236 | 43.7 | 45 | 57.7 | 1.76 | 1.09-2.84 | |
| Возраст на дату вступления в программу | |||||||
| 0-20 | 51 | 9.4 | 5 | 6.4 | .001 | 1.00 | Референс |
| 21-40 | 295 | 54.6 | 31 | 39.7 | 1.07 | 0.40-2.89 | |
| 41-60 | 171 | 31.7 | 31 | 39.7 | 1.85 | 0.68-5.00 | |
| >60 | 23 | 4.3 | 11 | 14.1 | 4.88 | 1.52-15.66 | |
| AMS | |||||||
| Нет | 53 | 9.8 | 9 | 11.5 | .636 | 1.00 | Референс |
| Да | 487 | 90.2 | 69 | 88.5 | 0.83 | 0.39-1.77 | |
| Меланома в прошлом | |||||||
| Нет | 317 | 58.7 | 24 | 30.8 | <.001 | 1.00 | Референс |
| Да | 223 | 41.3 | 54 | 69.2 | 3.20 | 1.92-5.33 | |
| Множественная меланома в прошлом | |||||||
| Нет | 484 | 89.6 | 61 | 78.2 | 1.00 | Референс | |
| Да | 56 | 10.4 | 17 | 21.8 | 2.41 | 1.32-4.41 | |
| Кол-во меланом до вступления в программу | |||||||
| 1 | 165 | 74.3 | 37 | 68.5 | .070 | 1.00 | Референс |
| 2 | 49 | 22.1 | 10 | 18.5 | 0.91 | 0.42-1.96 | |
| 3 | 5 | 2.3 | 3 | 5.6 | 2.68 | 0.61-11.70 | |
| 4 | 2 | 0.9 | 2 | 3.7 | 4.46 | 0.61-32.69 | |
| 5 | 1 | 0.5 | 2 | 3.7 | 8.92 | 0.79-100.98 | |
| Кол-во невусов | |||||||
| <50 | 40 | 7.4 | 4 | 5.1 | .058 | 1.00 | Референс |
| 50-100 | 200 | 37.0 | 18 | 23.1 | 0.90 | 0.29-2.80 | |
| 100-200 | 204 | 37.8 | 37 | 47.4 | 1.81 | 0.61-5.37 | |
| >200 | 96 | 17.8 | 19 | 24.4 | 1.98 | 0.63-6.29 | |
| >100 невусов | |||||||
| Нет | 240 | 44.4 | 22 | 28.2 | .007 | 1.00 | Референс |
| Да | 300 | 55.6 | 56 | 71.8 | 2.04 | 1.21-3.43 | |
| Фототип | |||||||
| I | 15 | 2.8 | 4 | 5.1 | .422 | 1.00 | Референс |
| II | 219 | 40.6 | 30 | 38.5 | 0.51 | 0.16-1.65 | |
| III | 284 | 52.6 | 43 | 55.1 | 0.57 | 0.18-1.79 | |
| IV | 22 | 4.1 | 1 | 1.3 | 0.17 | 0.02-1.68 | |
| Фототип | |||||||
| I-II | 234 | 43.3 | 34 | 43.6 | .966 | 1.00 | Референс |
| II-IV | 306 | 56.7 | 44 | 56.4 | 0.99 | 0.61-1.60 | |
| Лентиго | |||||||
| Нет | 214 | 39.6 | 26 | 33.3 | .286 | 1.00 | Референс |
| Да | 326 | 60.4 | 52 | 66.7 | 1.31 | 0.80-2.17 | |
| Удаленные новообразования | |||||||
| 0 | 211 | 39.1 | 0 | 0.0 | <.001 | – | – |
| 1 | 135 | 25.0 | 14 | 18.0 | 1.00 | 1.00 | |
| 2 | 70 | 13.0 | 14 | 18.0 | 1.93 | 1.93 | |
| 3 | 50 | 9.3 | 14 | 18.0 | 2.70 | 2.70 | |
| 4 | 35 | 6.5 | 9 | 11.5 | 2.48 | 2.48 | |
| 5 | 15 | 2.8 | 5 | 6.4 | 3.21 | 3.21 | |
| 6 | 10 | 1.9 | 7 | 9.0 | 6.75 | 6.75 | |
| >=7 | 14 | 2.6 | 15 | 19.2 | 10.33 | 10.33 | |
| CDKN2A | |||||||
| Отриц. | 239 | 44.3 | 61 | 78.2 | <.001 | 1.00 | Референс |
| Не провод. | 272 | 50.4 | 7 | 9.0 | 0.10 | 0.05-0.22 | |
| Положит. | 29 | 5.4 | 10 | 12.8 | 1.35 | 0.62-2.92 | |
| Возраст на дату включения |
36.2 | 12.8 | 42.4 | 15.5 | <.001 | 1.03 | 1.02-1.05 |
| Кол-во контролируемых новообр. |
17.2 | 8.2 | 24.2 | 13.0 | <.001 | 1.07 | 1.04-1.09 |
| Кол-во иссеченных новообр. |
1.5 | 1.9 | 4.3 | 3.5 | <.001 | 1.50 | 1.35-1.66 |
| Продолжительность наблюдения, мес. |
85.3 | 29.9 | 88.8 | 31.0 | 348 | 1.00 | 1.00-1.01 |
AMS — Синдром атипичного (диспластического невуса), CI — степень достоверности, MM — злокачественная меланома, OR — отношение шансов
Таблица 3. Анализ многофакторной логистической регрессии
| OR | 95 % CI | P значение | |
| Возраст на дату вступления в программу |
1.04 | 1.01-1.06 | .003 |
| Пол | |||
| Женский | 1.00 | Референтно | .500 |
| Мужской | 1.23 | 0.68-2.22 | |
| Меланома в прошлом | |||
| Нет | 1.00 | Референтно | .181 |
| Да | 1.55 | 0.81-2.97 | |
| >100 невусов | |||
| Нет | 1.00 | Референтно | .342 |
| Да | 1.37 | 1.37 | |
| Кол-во удаленных новообразований | 1.55 | 1.37-1.75 | <.001 |
| Фототип | |||
| I | 1.00 | Референтно | |
| II | 0.33 | 0.08-1.35 | .123 |
| III | 0.57 | 0.14-2.26 | .423 |
| IV | 0.03 | 0.00-0.76 | .033 |
| Мутация CDKN2A | |||
| Нет | 1.00 | Референтно | |
| Не проводилось | 0.15 | 0.06-0.37 | <.001 |
| Да | 1.39 | 0.53-3.68 | .505 |
AMS — Синдром атипичного (диспластического невуса),
CI — степень достоверности,
MM — злокачественная меланома,
OR — отношение шансов.
Для выявления злокачественной меланомы у пациентов с высоким риском заболевания предлагались различные способы, в том числе самообследование12,13, полное обследование поверхности кожи¹⁴, тотальное картирование тела3,15-19 и дерматоскопия20,21. Было продемонстрировано, что клиническое обследование не является точным при диагностике зарождающейся меланомы²², тогда как дерматоскопия показала повышение точности диагностики практически всех кожных новообразований, включая меланому20,21,23. В последние годы были накоплены доказательства в пользу применения цифровой дерматоскопии для контроля атипичных меланоцитарных новообразований2,6,7,24-30.
Цифровая дерматоскопия при наблюдении пациентов с высоким риском заболевания обеспечивает двойное преимущество, позволяя не пропустить злокачественную меланому, не обладающую дерматологическими признаками, и сокращая процент удаления доброкачественных новообразований (Таблица 4)².
Поскольку дерматоскопия точна не на 100 %, определенное количество подозрительных, но доброкачественных новообразований должно удаляться, чтобы не пропустить злокачественную меланому. В нашем исследовании в среднем за 8 лет наблюдений были иссечены менее двух доброкачественных новообразований на пациента, отношение злокачественности/доброкачественности меланомы составлял 1:10.7, коэффициент выявления меланомы ― 8,5 %, поддерживая факт, что цифровая дерматоскопия — эффективный и действенный метод ранней диагностики меланомы у пациентов с высоким риском заболевания.
Выявление новых клинически изменяющихся меланоцитарных новообразований у населения с высоким риском меланомы затруднено, и почти невозможно у пациентов с множественными невусами, кроме как вследствие сравнения результатов исследований методом полного картирования тела. Кроме того, хорошо известно, что злокачественная меланома чаще развивается на клинически нормальной коже, чем развивается на фоне меланоцитарных невусов³¹.
Таблица 4. Сравнение клинических результатов нашего исследования и результатов других рабочих групп
| Кол-во новообразований/ пациентов | Среднее кол-во новообразований на пациента | Средняя продолжительность наблюдения, мес. | % удаленных новообразований | Отношение Злокачественность/ доброкачественность |
Кол-во удалений ММ | % пациентов с диагнозом ММ во время программы наблюдения | |
| Haenssle и соавт, 6,7 2010, Germany |
11,137-688 | 16.18 | 46 | 10.9 | 1:8.5 | 10.4 | 11.4 |
| Haenssle и соавт, 6,7 2010, Germany |
600-405 | 1.48 | 23 | 9 | 1:3.4 | 22.2 | 3 |
| Fuller и соавт,4 2007, USA |
5945-297 | 20 | 22 | 5.4 | 1:53 PRL 1:95/NPRL 1:34.4 |
1.9 PRL 1.1/NPRL 2.75 |
2 |
| Haenssle и соавт, 25 2006, Germany |
7001-530 | 13.2 | 32.2 | 9.1 | 1:12 | 8.3 | 10 |
| Bauer и соавт, 26 2005, Germany (EPL) |
2015-196 | 10.28 | 25 | 1.6 | 1:15.5 | 6.1 | 1 |
| Robinson and Nickoloff,27 2004, USA |
2015-196 | 10.28 | 25 | 1.6 | 1:15.5 | 6.1 | 1 |
| Malvehy and Puig,5 2002, Barcelona |
3170-290 | 10.93 | 17.2 | 1.3 | 1:4.2 | 19 | 2.8 |
| Menzies и соавт,30 2001, Australia |
318-245 | 1.29 | 3 | 19.2 | 1:7.7 | 11.5 | 2.9 |
| Kittler и соавт,28 2000, Austria |
1862-202 | 9.21 | 12.6 | 4 | 1:8.4 | 10.7 | 4 |
| Наше исследование |
11,396-618 | 18.44 | 96 | 10.1 | 1:10.7 PRL 1:11.9/ NPRL 1:8.8 |
8.5 PRL 7.7/ NPRL 10.1 |
12.6 |
DFU – цифровое наблюдение;
EPL – эпилюминисцентный;
MM – злокачественная меланома;
NPRL – не зарегистрированное ранее новообразование;
PRL – ранее зарегистрированное новообразование.
Двухступенчатый метод цифровой дерматоскопии, использовавшийся в нашем отделении при наблюдении пациентов с высоким риском меланомы, заключается в сочетанном применении тотального картирования тела и цифровой дерматоскопии на каждом осмотре⁵. Мы уверены, что наш протокол представляет более полный подход, чем в других рабочих группах, где цифровая дерматоскопия сосредоточена исключительно на наблюдении зафиксированных ранее новообразований. С другой стороны, в протоколах цифровой дерматоскопии с тотальным картированием снимки тела фиксируются только на первых осмотрах, на последующих же поверхность кожи просто сравнивается с обзорными изображениями.
Уже в 2007 году Fuller и соавторы⁴ подчеркивали, что из большинства предшествовавших исследований неясно, пропущены ли некоторые злокачественные меланомы из-за того, что возникли на здоровой коже, или трансформировались из невусов, которые не были зафиксированы на дерматоскопическом обследовании, потому что общее количество злокачественных меланом у этих пациентов не сообщалось. В последнем исследовании только одна из шести злокачественных меланом, выявленных в среднем за 22 месяца, была определена методом цифровой дерматоскопии; с отношением злокачественности/доброкачественности меланомы 1:94 и 1:34.4 среди новообразований, зафиксированных или не зафиксированных ранее соответственно.
В нашем исследовании около 40 % злокачественных меланом, выявленных на контрольных осмотрах, относились к новообразованиям, которые прежде не были зафиксированы, потому что были вновь выявлены в ходе тотального картирования или присутствовали ранее, но не были атипическими и поэтому не включались в исследование. Соотношение злокачественных/доброкачественных меланом, согласно исследованию Fuller и соавторов⁴, ниже среди новообразований, не зафиксированных ранее (1:8.8 к 1:11.9).
10-летний опыт наблюдения пациентов с повышенным риском злокачественной меланомы, приведенный в исследовании Haenssle и соавторов6,7, заслуживает особого внимания. Как следует из Таблицы 4, общие данные относительно количества пациентов, наблюдаемых новообразований, процента иссеченных новообразований, отношения злокачественные/доброкачественные и пациентов с диагностированной в ходе исследования злокачественной меланомой очень схожи с нашими данными. Тем не менее некоторые различия очевидны: во-первых, наше наблюдение длилось в среднем 96 месяцев (8 лет), то есть более чем в два раза дольше, и дает больше основательных данных относительно долгосрочных наблюдений; и, во-вторых, в отличие от их исследования, мы решили не использовать данные об иссеченных на первых приемах новообразования, поскольку они не были частью наблюдений, оставив 16 злокачественных меланом для текущего анализа.
Haenssle и соавторы6,7 выявили большее количество случаев злокачественной меланомы в своем исследовании (127); если исключить 40 злокачественных меланом, которые они выявили после первого обследования, останется 87 злокачественных меланом, выявленных в ходе исследования, что схоже с нашими данными. Другим интересным отличием является процент злокачественных меланом, выявленных путем анализа изменений методом цифровой дерматоскопии, составляющий 36,7 % (32/87), исходя из их опыта, и 61,2 % (60/98) согласно нашим данным. Дальнейшие заключения сделать невозможно, поскольку количество участников различно.
Недавно Argenziano и соавторы³² сообщили, что злокачественная меланома может расти медленно, поэтому изменения можно увидеть только в результате длительного наблюдения. Наше наблюдение за новообразованиями продолжалось до 77 месяцев до того как потребовалось удаление, почти половина не подозрительных новообразований находились под контролем на протяжении более чем двух лет, прежде чем проявились признаки существенных изменений. Два открытия требуют особого внимания. Первое о том, что 75 % злокачественных новообразований с более чем 2-летним наблюдением до удаления носили характер in situ, и второе, что почти в 65 % случаев злокачественных меланом потребовалось более 2 лет наблюдений, в ходе которых невусы отсутствовали согласно гистопатологическим исследованиям (данные не приведены). Эти открытия подтверждают существования подгруппы медленно растущей злокачественной меланомы.
Хорошо известно, что цифровое дерматоскопическое исследование не только занимает время, но также является методом, требующим обучения, опыта и специального оборудования. Шансы на успех в цифровой дерматоскопии зависят главным образом от правильного отбора пациентов²⁹. В нашей группе участников, где 90 % пациентов страдали синдромом атопичного (диспластического) невуса и почти 45 % имели меланому в анамнезе, у одного из 8 злокачественная меланома развивалась во время исследования, что более чем в 1500 раз превышает ожидания. Не так неожиданно то, что процент пациентов с диагностированной в ходе наблюдения злокачественной меланомой увеличился до 7 % среди пациентов без личного анамнеза, до 18 и 23 % — у пациентов с одной или множественными злокачественными меланомами до вступления в исследование соответственно.
Длительность цифрового дерматоскопического исследования или возможность исключить пациента из программы, если иссечение не требовалось, было предметом спора. Согласно нашим выводам, злокачественная меланома может быть выявлена в любое время с момента вступления в программу цифрового исследования, а не только в ходе первых контрольных осмотров. Более того, риск диагностирования более чем одной злокачественной меланомы во время контрольных осмотров сравнительно велик у населения с высоким риском меланомы. В связи с этим пациентам из группы высокого риска требуется постоянное наблюдение.
Нет единого мнения относительно наиболее эффективных методов выявления меланомы у пациентов из группы высокого риска. Поскольку контрольные группы отсутствуют, мы не можем утверждать, является ли использование тотального картирования совместно с цифровой дерматоскопией более достоверными и эффективными, чем методы по отдельности. Недавно Goodson и соавторы¹⁸ сравнивали результаты тотального картирования и цифровой дерматоскопии при мониторинге невусов у схожей популяции с высоким риском меланомы и обнаружили, что мониторинг пациентов с риском меланомы с применением тотального картирования был связан с низким количеством биопсий и низким отношением доброкачественности/злокачественности меланомы, чем с использованием цифровой дерматоскопии и выявления новых изменяющихся новообразований, с высоким уровнем выявления злокачественной меланомы во время контрольных осмотров (4,4 % против 1,9 % соответственно). Используя двухступенчатый метод цифровой дерматоскопии, мы достигли более высокого коэффициента выявления меланомы (8,5 %) и более низкого отношения невус/ меланома (9.3 против 53 с цифровым методом и 22 с тотальным картированием). В нашем исследовании частота биопсии была выше, но это, возможно, связано с тем, что средний период наблюдений был в 4 раза дольше, и наши участники считались группой высокого риска из-за того, что коэффициент заболеваемости меланомой на пациента во время программы наблюдений был в 6 раз выше.
В заключение следует отметить, что тотальное картирование тела и цифровая дерматоскопия (двухступенчатый метод цифрового исследовании) у выбранной группы с высоким риском меланомы, способно выявлять меланому на ранних стадиях с низким числом удалений. Эта двойная опция полезна не только для определения злокачественной меланомы с незначительными дерматоскопическими признаками, но также для выявления как вновь появившейся, так и образованной из невуса, который не наблюдался дерматоскопически, меланомы. Для выявления медленно растущей меланомы требуется долгосрочное наблюдение. Исходя из нашего 10-летнего опыта меланому можно диагностировать в любое время, а не только на контрольных визитах, полагая что у пациентов с высоким риском дерматоскопическое исследование следует проводить регулярно.
1. Puig S, Argenziano G, Zalaudek I, Ferrara G, Palou J, Massi D, и соавт. Melanomas that failed dermoscopic detection: a combined clinicodermoscopic approach for not missing melanoma. Dermatol Surg 2007;33:1262-73.
2. Kittler H, Guitera P, Riedl E, AvramidisM, Teban L, Fiebiger M, и соавт. Identification of clinically featureless incipient melanoma using sequential dermoscopy imaging. Arch Dermatol 2006;142:1113-9.
3. Halpern AC. Total body skin imaging as an aid to melanoma detection. Semin Cutan Med Surg 2003;22:2-8.
4. Fuller SR, Bowen GM, Tanner B, Florell SR, Grossman D. Digital dermoscopic monitoring of atypical nevi in patients at risk for melanoma. Dermatol Surg 2007;33:1198-206.
5. Malvehy J, Puig S. Follow-up of melanocytic skin lesions with digital total-body photography and digital dermoscopy: a two-step method. Clin Dermatol 2002;20:297-304.
6. Haenssle HA, Korpas B, Hansen-Hagge C, Buhl T, Kaune KM, Rosenberger A, и соавт. Seven-point checklist for dermatoscopy: performance during 10 years of prospective surveillance of patients at increased melanoma risk. J Am Acad Dermatol 2010;62:785-93.
7. Haenssle HA, Korpas B, Hansen-Hagge C, Buhl T, Kaune KM, Johnsen S, и соавт. Selection of patients for long-term surveillance with digital dermoscopy by assessment of melanoma risk factors. Arch Dermatol 2010;146:257-64.
8. Pehamberger H, Steiner A, Wolff K. In vivo epiluminescence microscopy of pigmented skin lesions, I: pattern analysis of pigmented skin lesions. J Am Acad Dermatol 1987;17:571-83.
9. Stoltz W, Braun-Falco O, Bilek P, Landthaler M, Cognetta A. A color atlas of dermoscopy. Germany: Blackwell Science; 1994.
10. Argenziano G, Fabbrocini G, Carli P. Epiluminescence microscopy for the diagnosis of doubtful melanocytic skin lesions: comparison of the ABCD rule of dermatoscopy and a new 7-point checklist based on pattern analysis. Arch Dermatol 1998; 134:1563-70.
11. Puig S, Malvehy J, Badenas C, Ruiz A, Jimenez D, Cuellar F, и соавт. Role of the CDKN2A locus in patients with multiple primary melanomas. J Clin Oncol 2005;23:3043-5.
12. Berwick M, Begg CB, Fine JA, Roush GC, Barnhill RL. Screening for cutaneous melanoma by skin selfexamination. J Natl Cancer Inst 1996;88:17-23.
13. Oliveria SA, Christos PJ, Halpern AC, Fine JA, Barnhill RL, Berwick M. Evaluation of factors associated with skin selfexamination. Cancer Epidemiol Biomarkers Prev 1999;8:971-8.
14. Rigel DS, Friedman RJ, Kopf AW, Weltman R, Prioleau PG, Safai B, и соавт. Importance of complete cutaneous examination for the detection of malignant melanoma. J Am Acad Dermatol 1986;14:857-60.
15. Banky JP, Kelly JW, English DR, Yeatman JM, Dowling JP. Incidence of new and changed nevi and melanomas detected using baseline images and dermoscopy in patients at high risk for melanoma. Arch Dermatol 2005;141:998-1006.
16. Wang SQ, Kopf AW, Koenig K, Polsky D, Nudel K, Bart RS. Detection of melanomas in patients followed up with total cutaneous examinations, total cutaneous photography, and dermoscopy. J Am Acad Dermatol 2004;50:15-20.
17. Lucas CR, Sanders LL, Murray JC, Myers SA, Hall RP, Grichnik JM. Early melanoma detection: nonuniform dermoscopic features and growth. J Am Acad Dermatol 2003;48:663-71.
18. Goodson AG, Florell SR, Hyde M, Bowen GM, Grossman D. Comparative analysis of total body and dermatoscopic photographic monitoring of nevi in similar patient populations at risk for cutaneous melanoma. Dermatol Surg 2010;36:1087-98.
19. Risser J, Pressley Z, Veledar E, Washington C, Chen SC. The impact of total body photography onbiopsy rate in patients from a pigmented lesion clinic. J Am Acad Dermatol 2007;57:428-34.
20. Kittler H, Pehamberger H, Wolff K, Binder M. Diagnostic accuracy of dermoscopy. Lancet Oncol 2002;3:159-65.
21. Vestergaard ME, Macaskill P, Holt PE, Menzies SW. Dermoscopy compared with naked eye examination for the diagnosis of primary melanoma: a meta-analysis of studies performed in a clinical setting. Br J Dermatol 2008;159:669-76.
22. PizzichettaMA, Talamini R, Piccolo D, Argenziano G, Pagnanelli G, Burgdorf T, и соавт. The ABCD rule of dermatoscopy does not apply tosmallmelanocytic skinlesions.ArchDermatol 2001;137:1376-8.
23. Argenziano G, Soyer HP, Chimenti S, Talamini R, Corona R, Sera F, и соавт. Dermoscopy of pigmented skin lesions: results of a consensus meeting via the Internet. J Am Acad Dermatol 2003;48:679-93.
24. Schiffner R, Schiffner-Rohe J, Landthaler M, Stolz W. Long-term dermoscopic follow-up of melanocytic nevi: clinical outcome and patient compliance. Br J Dermatol 2003;149:79-86.
25. Haenssle HA, Krueger U, Vente C, Thoms KM, Bertsch HP, Zutt M, и соавт. Results from an observational trial: digital epiluminescence microscopy follow-up of atypical nevi increases the sensitivity and the chance of success of conventional dermoscopy in detecting melanoma. J Invest Dermatol 2006;126:980-5.
26. Bauer J, Blum A, Strohhacker U, Garbe C. Surveillance of patients at high risk for cutaneous malignant melanoma using digital dermoscopy. Br J Dermatol 2005;152:87-92.
27. Robinson JK, Nickoloff BJ. Digital epiluminescence microscopy monitoring of high-risk patients. Arch Dermatol 2004;140:49-56.
28. Kittler H, Pehamberger H, Wolff K, Binder M. Follow-up of melanocytic skin lesions with digital epiluminescencemicroscopy: patterns of modifications observed in early melanoma, atypical nevi, and common nevi. J Am Acad Dermatol 2000;43: 467-76.
29. Argenziano G, Mordente I, Ferrara G, Sgambato A, Annese P, Zalaudek I. Dermoscopic monitoring of melanocytic skin lesions: clinical outcome and patient compliance vary according to follow-up protocols. Br J Dermatol 2008;159: 331-6.
30. Menzies SW, Gutenev A, Avramidis M, Batrac A, McCarthy WH. Short-term digital surface microscopic monitoring of atypical or changing melanocytic lesions. Arch Dermatol 2001;137: 1583-9.
31. Weatherhead SC, Haniffa M, Lawrence CM. Melanomas arising from nevi and de novo melanomasedoes origin matter? Br J Dermatol 2007;156:72-6.
32. Argenziano G, Kittler H, Ferrara G, Rubegni P,Malvehy J, Puig S, и соавт. Slow-growing melanoma: a dermoscopy follow-up study. Br J Dermatol 2010;162:267-73.