Х. А. Хенсле1,*, К. Финк1,*, Р. Шнейдербауэр1, Ф. Тоберер1, Т. Бахл2, А. Блум3, А. Каллу4, А. Бен Хаджи Хассен5, Л. Томас6, А. Энк1 и Л. Ульманн7
Общие сведения: сверхточные нейронные сети (CNN) и технологии глубинного обучения могут облегчить процесс обнаружения меланомы. При этом не имеется данных о сравнении диагностической эффективности CNN с результатами диагностики большими группами дерматологов.
Хотите узнать цену аппарата FotoFinder aesthetics? Звоните нам +7 (495) 988-21-70!
Методы: архитектура Google Inception v4 CNN была обучена и прошла валидацию с использованием дерматоскопических изображений и соответствующих диагнозов. В сравнительном кросс-секционном дерматологическом исследовании применялся тестовый набор из 100 изображений (уровень I: только дерматоскопия; уровень II: дерматоскопия плюс клиническая информация и изображения). Основными оцениваемыми показателями были чувствительность, специфичность и площадь под ROC-кривой (AUC/ROC) при диагностической дихотомической классификации поражений, выполненной сетью CNN и международной группой из 58 дерматологов в ходе дерматологического исследования уровня I или II. Дополнительно оценивалась эффективность диагностики, проведенной дерматологами, при принятии ими врачебного решения, а также различия в результатах дерматологической диагностики в рамках исследования уровня I и II. Кроме того, результаты CNN сравнивались с показателями пяти лучших алгоритмов конкурса Международного симпозиума по биомедицинским изображениям (ISBI) 2016.
Результаты: дерматологи, принявшие участие в исследовании уровня I, при классификации поражений продемонстрировали следующие средние показатели (± стандартное отклонение) чувствительности и специфичности: 86,6% (± 9,3%) и 71,3% (± 11,2%), соответственно. При получении ими большего объема клинической информации (уровень II) чувствительность повысилась до 88,9% (± 9,6%, P = 0,19), а специфичность до 75,7% (± 11,7%, P < 0,05). ROC-кривая CNN показала более высокую специфичность: 82,5% по сравнению с результатами дерматологов уровня I (71,3%, P < 0,01) и уровня II (75,7%, P < 0,01) при их показателях чувствительности 86,6% и 88,9%, соответственно, Площадь под ROC-кривой CNN была больше средней площади под ROC-кривой дерматологов (0,86 против 0,79, P < 0,01). Результаты сети CNN были близки к показателям трех лучших алгоритмов конкурса ISBI 2016.
Заключение: мы первые исследователи, которые сравнили диагностические показатели CNN с результатами диагностики, выполненной большой международной группой из 58 дерматологов, включающей 30 экспертов. Диагностическая эффективность сети CNN превосходила результаты большинства дерматологов. Использование CNN при классификации изображений будет полезно любому врачу, независимо от его опыта работы. Номер клинического испытания: данное исследование было зарегистрировано в Немецком реестре клинических испытаний (DRKS-Study-ID: DRKS00013570; https://www.drks.de/drks_web/).
Ключевые слова: меланома, меланоцитарный невус, дерматоскопия, сверточная нейронная сеть глубинного обучения, компьютерный алгоритм, автоматизированное обнаружение меланомы.
За последние несколько десятилетий меланома стала серьезной проблемой в области общественного здравоохранения (1). Постоянный рост числа заболеваний и смертности от меланомы способствовал тому, что все больше внимания стало уделяться раннему выявлению и профилактике (2). Несколько метаанализов показало, что дерматоскопия значительно улучшает диагностическую точность обследования, проводимого «невооруженным глазом» (3–5). Однако дерматологи и другие врачи, изучившие различные дерматоскопические алгоритмы, демонстрируют показатели средней чувствительности при выявлении меланомы в основном на уровне < 80% (6, 7).
В последние годы были исследованы несколько стратегий автоматического компьютерного анализа изображений в качестве вспомогательного средства для врачей с целью обеспечения высокой и широко воспроизводимой диагностической точности при скрининге меланомы (8–11). Эти подходы были ограничены использованием «искусственных» критериев дерматоскопической сегментации при диагностике меланомы (например, множество цветов, определенные морфологические структуры в виде полос/псевдоподий, нестандартные сосудистые структуры) (12).
В своей знаковой публикации авторы Esteva et al. сообщили об обучении и тестировании сверточной нейронной сети глубинного обучения (CNN) в направлении классификации на основе изображений в 2017 году (13). В данном случае сеть CNN не ограничивалась критериями искусственной сегментации, а деконструировала цифровые изображения до уровня пикселей и создавала собственные диагностические подсказки. Как и в исследовании, представленном в настоящем документе, авторы использовали предварительно обученную архитектуру GoogleNet Inception CNN (14), дополнительно прошедшую обучение на более чем 100 000 цифровых изображений и соответствующих метках заболеваний.
Цель настоящего исследования состояла в том, чтобы обучить, провести валидацию и протестировать CNN глубинного обучения в направлении диагностической классификации дерматоскопических изображений поражений меланоцитарного происхождения (меланома, доброкачественные невусы) и сравнить результаты с диагностическими выводами группы из 58 дерматологов.
Исследование было одобрено местным этическим комитетом и проведено в соответствии с принципами Хельсинкской декларации.
Подробная информация о методах, относящихся к архитектуре и обучению CNN, содержится в документе «Дополнительные методы», доступном на сайте журнала «Annals of Oncology».
Мы использовали и специально обучали модифицированную версию архитектуры Google Inception v4 CNN (Рисунок S1, см. на сайте Annals of Oncology) (14).
Мы создали тестовый набор из 300 изображений, включающий 20% меланом (in situ и инвазивных) всех участков тела и всех частых гистотипов, а также 80% доброкачественных меланоцитарных невусов различных подтипов и участков тела, включая так называемые «симуляторы меланомы» (Таблица S1, см. на сайте Annals of Oncology).
Поскольку почти две трети доброкачественных невусов были неудаленными поражениями, подтвержденными последующими осмотрами, этот набор данных представлял спектр меланоцитарных поражений, которые обычно встречаются в повседневной клинической практике. Изображения тестового набора «300» были получены из прошедшей валидацию библиотеки высококачественных изображений факультета дерматологии Гейдельбергского университета, Германия.
Для получения изображений использовались различные комбинации камеры и дерматоскопа. Не допускалось совпадение наборов данных для обучения/валидации и тестирования.
Перед тестированием CNN два опытных дерматолога проспективно отобрали 100 изображений из набора «300» для повышения диагностической сложности (Таблица S2, см. на сайте Annals of Oncology). Набор «100» использовался для тестирования CNN в сравнении с диагностикой, выполняемой дерматологами в рамках глобального дерматологического исследования. Участники (172 человека) приглашались посредством списков рассылки Международного общества дерматоскопии, и 58 из них (33,7%) отправили в ответ заполненные формы для участия. Данные участники указали свой уровень опыта в дерматоскопии: «Начинающий» < 2 лет опыта, «Квалифицированный» 2–5 лет опыта, «Эксперт» ≥ 5 лет опыта.
В исследовании уровня I дерматологам предоставили только дерматоскопическое изображение и предложили поставить дихотомический диагноз (меланома, доброкачественные невусы), а также принять врачебное решение (удаление, кратковременное наблюдение, никаких действий не требуется). Через 4 недели те же участники поставили диагноз и приняли врачебное решение в рамках исследования уровня II, в котором помимо дерматоскопических изображений была предоставлена дополнительная клиническая информация и те же 100 изображений, но в увеличенном формате – крупным планом.
Мы использовали и другой набор из 100 изображений, созданный в рамках проекта по меланоме Международного сообщества по визуализации кожи (ISIC) в связи с проведением Международного симпозиума по биомедицинской визуализации (ISBI) 2016. При помощи этого набора было осуществлено прямое сравнение нашей CNN с международными алгоритмами первой пятерки победителей конкурса (15).
Основными оцениваемыми показателями были чувствительность, специфичность и площадь под ROC-кривой (AUC/ROC) при диагностической дихотомической классификации поражений, выполненной сетью CNN и дерматологами в ходе дерматологического исследования уровня I или II . Дополнительно оценивалась эффективность диагностики, проведенной дерматологами, при принятии ими врачебного решения, а также различия в результатах дерматологической диагностики в рамках исследования уровня I и II. Для расчета и чувствительности, и специфичности при принятии врачебного решения был дополнительно включен вариант «краткосрочного наблюдения».
Было подсчитано среднее количество (процент) всех поражений и всех меланом, по которым было показано последующее наблюдение, частота удаления доброкачественного невуса (число удаленных невусов/число всех невусов) и количество, подлежащее удалению (NNE; количество вырезанных поражений/количество удаленных меланом).
При дихотомической классификации злокачественных и доброкачественных поражений сеть CNN выставляла «оценку злокачественности» в диапазоне от 0 до 1 с точкой отсечения на уровне > 0,5. Для сравнения показателей CNN с результатами дерматологов был применен двусторонний t-критерий с одним образцом, и рассчитана специфичность на уровне средней чувствительности среди дерматологов и площадь ROC-кривой CNN в сравнении со средней площадью под ROC-кривой среди дерматологов.
По дихотомичным прогнозам дерматологов площадь под ROC-кривыми эквивалентна средней чувствительности и специфичности. Были использованы описательные статистические данные, такие как частота, среднее значение, диапазон и стандартное отклонение. Для оценки различий в диагностической эффективности дерматологов в рамках I и II уровня исследования использовались двусторонние t-тесты. Результаты считались статистически значимыми на уровне P < 0,05. Все анализы проводились с использованием SPSS Version 24 (IBM, SPSS; Чикаго, Иллинойс).
Семнадцать (29,3%) из 58 участвующих дерматологов из 17 стран указали, что являются «начинающими» в области дерматоскопии (< 2 лет опыта), в то время как 11 (19%) и 30 (51,7%) заявили, что они «квалифицированные» специалисты (2–5 лет опыта) или «эксперты» (> 5 лет опыта), соответственно. Из соображений практической целесообразности дерматологам было предложено изучить только тестовый набор «100».
Таблица 1. Результаты исследования уровня I и II.
ROC — график соотношения объектов бинарной классификации.
Уровень I: дерматологам-участникам исследования были предоставлены только дерматоскопические изображения.
Уровень II: дерматологам-участникам была дополнительно предоставлена клиническая информация и увеличенные изображения.
«Эксперт»: дерматолог указал, что имеет > 5 лет опыта в сфере дерматоскопии.
«Квалифицированный»: дерматолог указал, что имеет 2–5-летний опыт в сфере дерматоскопии.
«Начинающий»: дерматолог указал, что имеет < 2 лет опыта в сфере дерматоскопии.
Диагностическая классификация в дерматологическом исследовании I уровня (только дерматоскопия). Средняя (± стандартное отклонение (SD)) чувствительность и специфичность среди 58 дерматологов при дихотомической классификации поражений набора «100» в рамках исследования уровня I составила 86,6% (± 9,3%) и 71,3% (± 11,2%), соответственно (Таблица 1). Эти данные соответствуют средней (± SD) площади под ROC-кривой на уровне 0,79 (± 0,06). Эксперты в области дерматоскопии показали значительно более высокую среднюю чувствительность, специфичность и площадь под ROC-кривой, чем начинающие (89% (± 9,2%), 74,5% (± 12,6%), 0,82 (± 0,06) против 82,9% (± 7,1%), 67,6% (± 6,3 %), 0,75 (± 0,04), соответственно; все P <0,02; Таблица 1).
Врачебные решения в рамках дерматологического исследования уровня I (только дерматоскопия). В качестве вариантов врачебных решений участникам было предложено (i) удаление, (ii) краткосрочное последующее наблюдение или (iii) никаких действий не требуется. В этом случае средняя (± SD) чувствительность и площадь под ROC-кривой значительно увеличились: до 98,8% (± 2,9%, P < 0,01) и 0,82 (± 0,07, P < 0,03), соответственно (Таблица 1). Напротив, специфичность значительно снизилась с 71,3% до 64,6% (± 13,6%, P <0,01). Подобные изменения наблюдались среди участников всех уровней опыта.
Среди всех дерматологов в среднем (± SD) выбор опции удаления доброкачественных невусов составил 35,4% (± 13,6%), а выбор наблюдения за поражением – 33,5% (± 11,7%). Дерматологи включили в последующее наблюдение среднее количество (± SD) 1,9 (± 1,6) меланом и достигли NNE 2,3 (± 0,6). При большем опыте дерматолога наблюдалось значительное снижение частоты случаев выбора опции удаления доброкачественного невуса, наблюдения за поражением и количества меланом, находящихся под последующим наблюдением (все Р <0,05). Показатель NNE также немного улучшился в случае большего опыта дерматолога, однако, не достиг статистической значимости.
Диагностическая классификация в дерматологическом исследовании уровня II (дерматоскопия и клиническая информация). Добавление клинической информации (возраст, пол и участок на теле) и изображений крупным планом улучшило средний показатель чувствительности, специфичности, полученный дерматологами (± SD), и площадь под ROC-кривой до 88,9% (± 9,6%, P = 0,19), 75,7% (± 11,7%, Р <0,05) и 0,82 (± 0,06, Р < 0,01),соответственно (Таблица 1). Эти изменения были основаны исключительно на значительных улучшениях среди «начинающих» и «квалифицированных» дерматологов. Значимого положительного воздействия дополнительной клинической информации и увеличенных изображений на результаты «экспертов» в сфере дерматоскопии продемонстрировано не было.
Выполняя задачу о принятии врачебного решения в рамках исследования уровня II, дерматологи улучшили свои результаты дихотомической классификации уровня II до следующей средней (± SD) чувствительности, специфичности и площадью под ROC-кривой: 98,6% (± 2,8%, P <0,01), 66,7% (± 12,4%, P <0,01) и 0,83 (± 0,06, P =0,76) (Таблица 1).
Однако мы не обнаружили существенных различий между этими результатами и показателями врачебных решений исследования уровня I. Среднее (± SD) число меланом, включенных в краткосрочное последующее наблюдение, снизилось с 1,9 (± 1,6) до 1,3 (± 1,5) меланом (P = 0,03), а показатель NNE оставался неизменным при 2,3 доброкачественных невусах, удаленных для выявления одной меланомы.
По врачебным решениям в рамках исследования уровня II больший опыт («эксперты» по сравнению с «начинающими») был связан со значительно лучшим показателем средней (± SD) площади под ROC-кривой (0,84 (± 0,06) против 0,79 (± 0,06), P = 0,03). По другим параметрам врачебных решений в рамках исследования уровня II не продемонстрировано существенных различий в результатах дерматологов с разным опытом.
На коробчатых диаграммах на Рисунке 1 показано распределение оценок вероятности меланомы по доброкачественным невусам, меланомам in situ и инвазивным меланомам. Когда вышеупомянутые параметры были применены к тестовому набору «100», чувствительность, специфичность и площадь под ROC-кривой составили 95%, 63,8% и 0,86, соответственно.
Рисунок 1.
Оценки CNN о вероятности меланомы (диапазон 0–1) по доброкачественным невусам (зеленый) по сравнению с in situ (оранжевый) или инвазивными меланомами (красный) изображены в виде коробчатых диаграмм по тестовым наборам «100» и «300». Баллы ближе к 1 указывают на более высокую вероятность меланомы. Верхняя и нижняя границы блоков обозначают 25-й и 75-й процентили, а медиана обозначена пересечением линий верхнего и нижнего блока. «Усы» указывают на полный диапазон вероятностных оценок.
Статистический анализ выявил значительно отличающиеся оценки вероятности меланомы при сравнении доброкачественных поражений с in situ или инвазивными меланомами (P< 0,001). Тем не менее, оценки вероятности меланомы по in situ и инвазивным меланомам не показали существенных различий (набор «300» P = 0,84, набор «100» P = 0,24).
По более крупному тестовому набору «300», включающему проще диагностируемые поражения, чувствительность, специфичность и площадь под ROC-кривой составляли 95%, 80% и 0,95, соответственно. Обе ROC-кривые изображены на Рисунках 2А и В.
В качестве эталона для сравнения с CNN мы использовали среднюю чувствительность среди дерматологов (86,6%) при диагностической классификации в рамках исследования уровня I (Рисунок 2А). При этой чувствительности специфичность CNN была выше (82,5%), чем средняя специфичность среди дерматологов (71,3%, P < 0,01). Кроме того, в исследовании уровня I площадь под ROC-кривой CNN (0,86) была больше, чем средняя площадь под ROC-кривой среди дерматологов (0,79, P < 0,01).
Когда дерматологи получили больше клинической информации и увеличенные изображения (исследование уровня II), их диагностические показатели улучшились. При использовании средней чувствительности дерматологического исследования уровня II 88,9% в качестве рабочей точки на ROC-кривой CNN, специфичность CNN составила 82,5%, что было значительно выше, чем средняя специфичность по дерматологам: 75,7% (P < 0,01). Опять же, площадь под ROC-кривой CNN (0,86) была больше, чем средняя площадь под ROC-кривой среди дерматологов (0,82, P < 0,01).
Непосредственное сравнение ROC-кривых нашей CNN с международными индивидуальными алгоритмами первой пятерки конкурса ISBI 2016 (15) показано на Рисунке 3. При площади под ROC-кривой 0,79 сеть CNN, представленная в настоящем документе, была среди трех лучших алгоритмов конкурса ISBI 2016 с почти полностью совпадающими ROC-кривыми.
Показатели заболеваемости меланомой неуклонно растут среди представителей большинства светлокожих популяций. Согласно прогнозам, эти показатели будут расти и в дальнейшем (2). Несмотря на различные уровни подготовки и опыта врачей, занимающихся ранним выявлением меланомы, желательно получить воспроизводимо высокую точность диагностики. С этой целью мы обучили и протестировали сверточную нейронную сеть (CNN) глубинного обучения в направлении различения дерматоскопических изображений меланомы и доброкачественных невусов.
Мы первые исследователи, которые сравнили диагностические показатели CNN с результатами большой международной группы из 58 дерматологов из 17 стран, включая 30 экспертов с более чем 5-летним опытом в области дерматоскопии. Когда дерматологам были предоставлены только дерматоскопические изображения (исследование уровня I), сеть CNN значительно лучше выполнила дихотомическую классификацию поражений по сравнению с дерматологами.
Тем не менее, в реальных клинических условиях дерматологи при принятии врачебных решений обладают большим объемом клинической информации. Поэтому мы исследовали воздействие дополнительной клинической информации и наличие изображений, сделанных крупным планом, и обнаружили значительно более высокую диагностическую эффективность среди дерматологов (исследование уровня II). Однако при улучшенной средней чувствительности (88,9%) дерматологи все же продемонстрировали специфичность, уступающую CNN (75,7% против 82,5%, P < 0,01).
Наши данные ясно показывают, что алгоритм CNN может быть подходящим инструментом, помогающим обнаруживать меланомы независимо от индивидуального уровня подготовки и опыта врача. Следует отметить, что в исследовании уровня I тринадцать (22,4%) из 58 дерматологов продемонстрировали несколько более высокую диагностическую эффективность, чем CNN.
Мы сознательно выбрали дихотомическую классификацию поражений дерматологами в наборе «100» в качестве основного оцениваемого показателя для сравнения с CNN. Тем не менее, можно утверждать, что ежедневную задачу дерматологов при скрининге рака кожи в большей степени представляют «врачебные решения», а не «диагностическая классификация».
Помимо опций «удаления» и «никаких действий не требуется» имелась третья опция врачебного решения: краткосрочное последующее обследование, которое включили в отношении единичных поражений с более высокой степенью атипии (например, разнообразные оттенки цвета, асимметрия в форме или заметная сетка), не требующих немедленного удаления при подозрении на меланому (16). Статистическая оценка опции последующего наблюдения сопряжена с некоторыми трудностями.
С одной стороны, было показано, что краткосрочное наблюдение является эффективной мерой, позволяющей дифференцировать ранние меланомы и доброкачественные невусы путем выявления динамических изменений (17–19). С другой стороны, слишком частое использование такой «темной лошадки» как последующее наблюдение может (i) применяться для сокрытия недостатка дерматоскопической экспертизы, (ii) быть практически неосуществимым в повседневной клинической практике и (iii) отсрочить удаление меланомы.
Поэтому мы дополнительно включили опцию последующего наблюдения в расчет чувствительности (меланомы под наблюдением: «истинные положительные») и специфичности (невусы под наблюдением: «истинные отрицательные»).
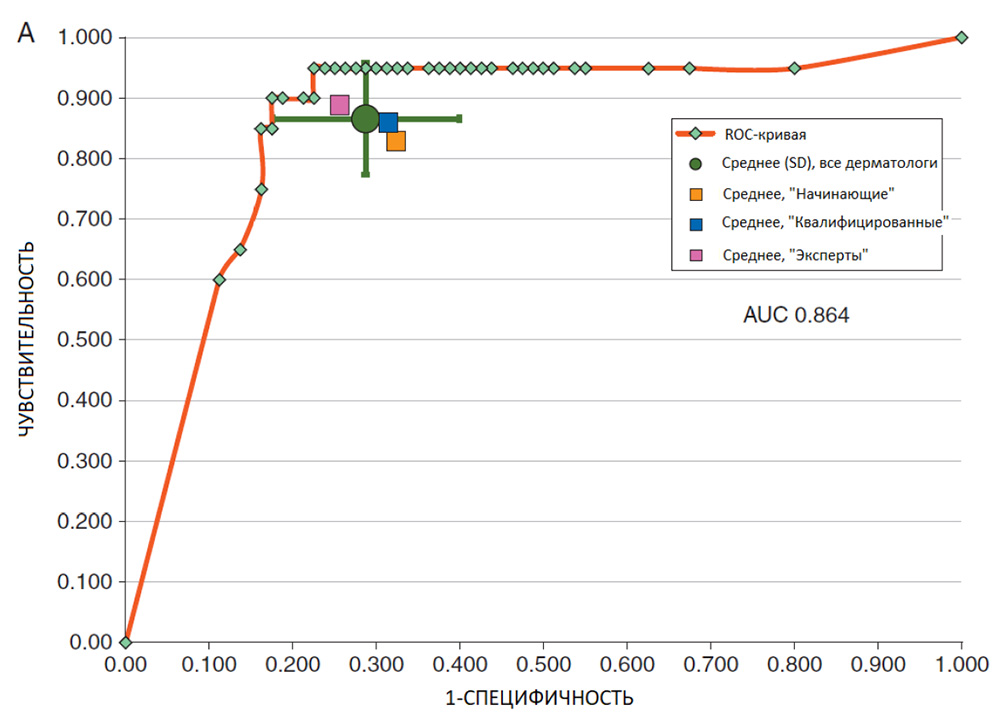
Рисунок 2.
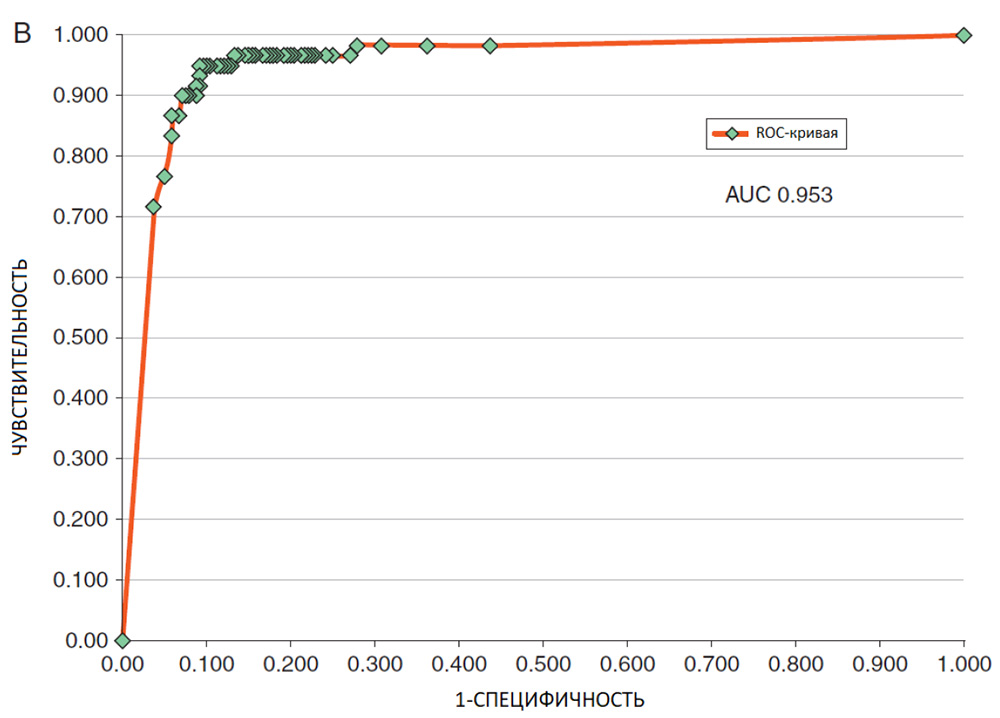
(A) ROC-кривая CNN по отношению к средней (± SD) чувствительности и специфичности среди всех дерматологов (среднее: зеленый круг; ± SD: зеленые индикаторы ошибок) в наборе «100» (дихотомическая классификация, исследование уровня I) и средняя чувствительность и специфичность среди дерматологов в зависимости от их опыта. (B) ROC-кривая CNN в наборе «300».
Тем не менее, мы также проверили детали выбора опции последующего наблюдения и обнаружили, что дерматологи отбирали примерно треть поражений для последующего наблюдения, в то время как среднее абсолютное количество меланом под наблюдением находилось в диапазоне 1,3-1,9. Как и ожидалось, при большем опыте врача и добавлении клинической информации наблюдалось снижение частоты выбора опции последующего наблюдения.
Важно отметить, что различия в уровне сложности, присущие любому тестовому набору изображений, будут напрямую влиять на диагностическую эффективность алгоритмов и врачей. Поэтому для реализации возможности сопоставимости различных компьютерных алгоритмов крайне важно включить большую группу дерматологов с различным уровнем опыта, а также создать и использовать открытые общедоступные наборы данных, такие как наборы ISIC (15).
В отличие от Marchetti et al. (15) другие авторы не использовали «эталонные» наборы изображений, и только несколько исследований включали небольшое количество участников для сравнения с разработанными ими компьютерными алгоритмами (13, 20). Кроме того, по возможности, наборы должны включать поражения различных участков тела и гистотипов. Как показано в Таблицах S1 и S2 (см. на сайте Annals of Oncology), наборы «100» и «300» соответствовали этим требованиям и позволяли создать менее «искусственную» учебную среду.
Рисунок 3.
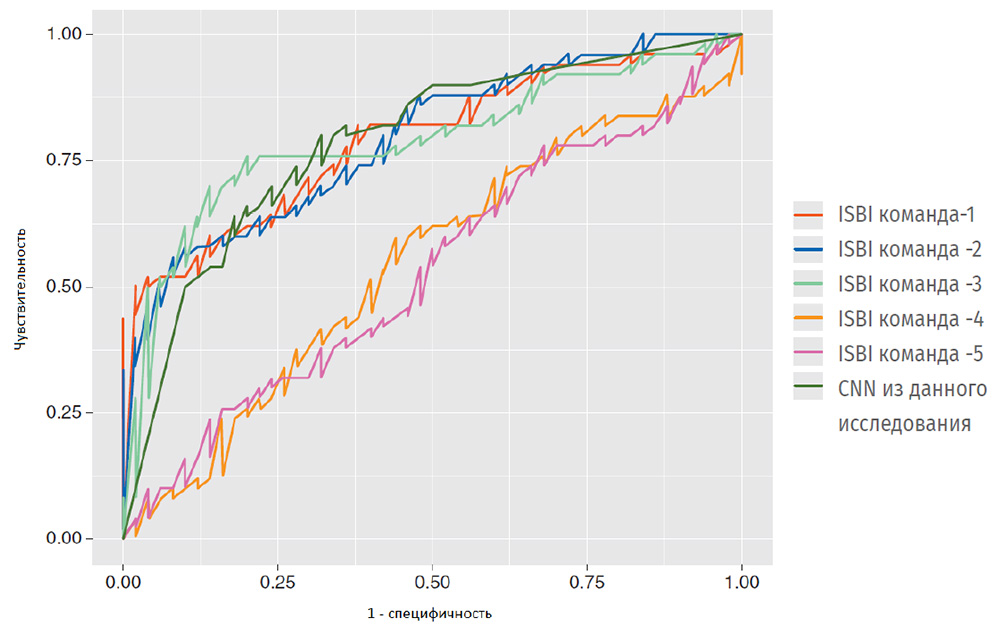
Сравнение ROC-кривых CNN, описанных в данном исследовании (темно-зеленая линия), с пятью лучшими алгоритмами конкурса Международного симпозиума по биомедицинской визуализации (ISBI) 2016 (18). Площадь под ROC-кривой в порядке убывания: ISBI команда-2: 0,7956; ISBI команда-1: 0,7928; ISBI команда-3: 0,7892; CNN в данном исследовании: 0,7868; ISBI команда-4: 0,5460; ISBI команда-5: 0,5324.
Наше исследование показывает ряд ограничений, которые могут препятствовать более широкому обобщению. Во-первых, как и во всех подобных исследованиях, условия для тестирования диагностической эффективности дерматологов были искусственными, поскольку им не нужно было бояться отрицательных последствий потенциального необнаружения меланомы.
Во-вторых, тестовые наборы нашего исследования не отражали полного спектра поражений (например, таких, как пигментированная форма базальноклеточного рака или себорейный кератоз).
В-третьих, в результате недостатка изображений, прошедших валидацию, наблюдалась нехватка меланоцитарных поражений других типов кожи и генетического происхождения.
В-четвертых, как показано в более ранних подобных исследованиях, оперирующие врачи могут не следовать рекомендациям CNN, которым они не полностью доверяют, что может снизить заявляемую диагностическую эффективность (21).
Помимо подтверждения наших результатов при помощи более крупных и разнообразных тестовых наборов, необходимы проспективные исследования с участием пациентов и врачей, вовлеченных в скрининг рака кожи.
В заключение хотелось бы отметить следующее. Результаты нашего исследования демонстрируют, что надлежащим образом натренированная сеть CNN глубинного обучения способна к высокоточной диагностической классификации дерматоскопических изображений меланоцитарного происхождения. Используя также результаты дерматологических исследований уровня I и II, мы смогли показать, что диагностическая эффективность CNN превосходила результаты большинства – хотя и не всех – дерматологов. И хотя настройка и обучение архитектуры CNN является сложной задачей, ее внедрение в системы цифровой дерматоскопии или приложения для смартфонов может быть осуществлено с легкостью. Таким образом, классификация изображений при помощи сети CNN может помочь в работе врачам с любым уровнем подготовки и опыта.
Мы хотели бы поблагодарить нижеуказанных врачей-дерматологов, которые активно и добровольно уделяют много времени участию в исследовании уровня I и II.
Фамилии приведены в алфавитном порядке: Кристина Альт, Моника Аренбергерова, Ренато Бакос, Энн Бальцер Инес Бертлих, Андреас Блюм, Терезия Бокор- Биллманн, Джонатан Боулинг, Наира Брагироли, Ральф Браун, Кристина Будер-Бахая, Тимо Буль, Лёбомира Влахова, Александр Вальд, Юлия Винклер, Присцила Волбинг, Дэвид Дельтген, Кристина Георгия, Ирис Залаудек, Орасио Кабо, Раймондс Карлс, Хироши Кога, Юрген Креуш, Лев Кабрижан, Анна Классен, Эмилиос Лаллас, Павел Маженка, Эш Маргхобик, Чезаре Массокевен, Мали Массоне, Лали Мали Фолькер Мейер, Анна Нойбергер, Кари Нильсен, Маргарет Оливьеро, Риккардо Пампена, Джон Паоли, Эрика Павлик, Барбар Рао, Адриана Рендон, Тереза Руссо, Ахмед Садек, Кинга Самхабер, Лукас Тренхойзер, Ик Лара-Елена Хаким- Мейбоди, Сюзанна Ханнер, Франциска Хартманн, Джулия Хартманн, Георг Хаус, Эльти Ходжа, Насье Цевич, Роланд Шнайдербауэр, Анисса Швайцер, Феррер.
Некоторые участники предпочли остаться анонимными, и мы также благодарим этих коллег за их приверженность. Кроме того, благодарим Международное общество дерматоскопии (IDS) за предоставление списка рассылки, благодаря которому мы смогли пригласить дерматологов для участия в исследовании.
Рассмотрено и одобрено этическим комитетом медицинского факультета Гейдельбергского университета (номер одобрения S-629/2017).
Не было получено какого-либо специального гранта на данное исследование от организаций государственного, коммерческого или некоммерческого сектора.
Автор Х.А.Х. получил гонорары и/или покрытие командировочных расходов от компаний, занимающихся разработкой устройств для скрининга рака кожи: Scibase AB, FotoFinder Systems GmbH, Heine Optotechnik GmbH, Magnosco GmbH. Автору К.Ф. были компенсированы командировочные расходы компанией Magnosco GmbH. Остальные авторы заявили об отсутствии конфликта интересов.